Виды трансплантации костного мозга и иммунотерапия
Содержание:
- Голова
- Трансплантация в Энциклопедическом словаре:
- Типирование тканей.
- Пересадка почки.
- Что изменится с принятием нового закона о донорстве?
- Проблемы «черной» трансплантологии
- Поведение после процедуры
- Почему могут не прижиться эмбрионы?
- Селезенка
- История развития трансплантологии
- Консервация органов.
- История трансплантации органов
- Виды трансплантации органов и тканей
- А если я не хочу быть донором после смерти?
Голова
Image caption
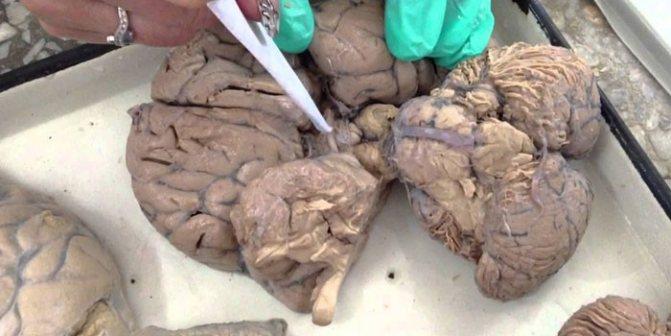
Мозг — самая сложная биологическая структура в организме
Трансплантация головы невозможна и вряд ли станет возможной в ближайшем будущем — хирургия сосредоточена на наиболее прагматичных медицинских результатах.
«Мы должны сосредоточить внимание на том, чего мы можем достичь. И мы многого достигли за последние 50 лет в плане пересадки почти каждой части тела ниже шеи», — говорит доктор Габриэль Ониску, хирург-консультант по трансплантации в Королевской больнице Эдинбурга и секретарь Европейского общества трансплантации органов
Жизнь в зоне смерти: как итальянская пара стала легендой альпинизма
Доктор Лорна Мейсон, хирург-трансплантолог и президент Британского трансплантационного общества соглашается с тем, что в каждом случае врачи сосредоточены на том, как сохранить жизнь большого количества людей и выбрать наиболее реалистичные варианты.
Кроме очевидных философских споров (будет ли тело получать новый мозг, или мозг получит новое тело?), основная сложность такого типа операции заключается в том, чтобы соединить головной мозг со спинным.
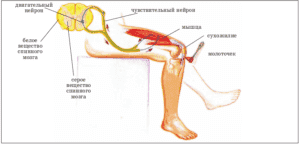
Большинство трансплантационных операций заключается в успешном соединении кровеносных сосудов, но спинной мозг — ответственный за телодвижения — это сеть высокоспециализированных клеток, называемых нейронами или нервными клетками.
Image caption
Нейроны отличаются от других клеток в организме
Этот тип клетки передает информацию с помощью электрических и химических сигналов, и, если они повреждены, их можно заменить другими или заново соединить.
Это объясняет, почему тяжелые повреждения спинного мозга до сих пор в основном являются необратимыми.
Умершая девочка-донор спасла восемь жизней
Доктор Мейсон говорит, что в случаях поражения головного мозга более реалистичные варианты, например замена клеток там, где это возможно.
Ученые разрабатывают клеточные терапии, которые позволят нейронам восстанавливаться и развиваться.
«Клеточная терапия может остановить или, в некоторых случаях, даже вылечить дегенеративное заболевание клеточной ткани мозга или нервной системы, — говорит Мейсон. — Такое лечение может быть полезным для пациентов с деменцией или рассеянным склерозом».
Трансплантация в Энциклопедическом словаре:
Трансплантация — (от ср.-век. лат. transplantatio — пересаживание) -..1) учеловека и животных пересадка органов, тканей. Как хирургический методизвестна с глубокой древности. Используется трансплантация кожи, мышц,нервов, роговицы глаза, жировой и костной ткани, костного мозга, сердца,почек и др. Особый вид трансплантации — переливание крови. В биологии,экспериментальной (на животных) и клинической медицине применяют ауто-(трансплантация собственных тканей), гомо- (трансплантация от донора тогоже вида) и гетеротрансплантацию (трансплантация от донора другого вида,напр. собаке от кролика)…2) У растений — пересадка части растения надругое место материнского растения или на другое растение. Применяется всадоводстве (см. Прививки) и экспериментальных исследованиях.
Типирование тканей.
Как и при переливании крови (которое тоже можно рассматривать как пересадку органа), чем более «совместимы» донор и реципиент, тем выше вероятность успеха, поскольку трансплантат будет для реципиента менее «чужим». В оценке такой совместимости сделаны большие успехи, и в настоящее время удается определять различные группы HLA-антигенов. Так, классифицируя, или «типируя», антигенный набор лимфоцитов донора и реципиента, можно получить сведения о совместимости их тканей.
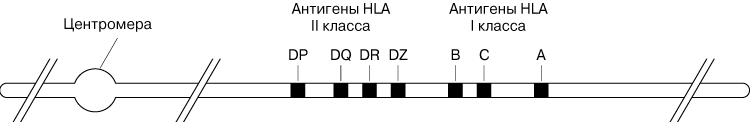
Известно семь разных генов гистосовместимости. Все они расположены близко друг к другу на одном участке ДНК и образуют т.н. главный комплекс гистосовместимости (MHC, от англ. – major histocompatibility complex) одной (6-й) хромосомы. Местоположение, или локус, каждого из этих генов обозначают буквами (соответственно A, B, C и D; локус D несет 4 гена). Хотя у индивида каждый ген может быть представлен только двумя разными аллелями, в популяции таких аллелей (и соответственно HLA-антигенов) множество. Так, в локусе A выявлено 23 аллеля, в локусе B – 47, в локусе C – 8 и т.д. Антигены HLA, кодируемые генами локусов A, В и C, называют антигенами класса I, а кодируемые генами локуса D – антигенами класса II (см. диаграмму). Антигены класса I химически сходны, но существенно отличаются от антигенов класса II. Все HLA-антигены представлены на поверхности разных клеток в разных концентрациях
При типировании тканей основное внимание уделяется идентификации антигенов, кодируемых локусами A, B и DR
Поскольку гены гистосовместимости расположены близко друг к другу на одной и той же хромосоме, участок МНС каждого человека почти всегда передается по наследству целиком. Хромосомный материал каждого из родителей (половина всего материала, наследуемого потомком) называется гаплотипом. Согласно законам Менделя, 25% потомков должны быть идентичными по обоим гаплотипам, 50% – по одному из них и у 25% – не должен совпадать ни один гаплотип. Сиблинги (братья и сестры), идентичные по обоим гаплотипам, не имеют различий в системе гистосовместимости, поэтому пересадка органов от одного из них другому не должна вызывать никаких осложнений. И наоборот, поскольку вероятность обладания обоими идентичными гаплотипами у лиц, не являющихся родственниками, чрезвычайно мала, при пересадке органов от одного из таких лиц другому почти всегда следует ожидать реакции отторжения.
Кроме HLA антигенов, при типировании определяют и антитела в сыворотке крови реципиента к этим антигенам донора. Такие антитела могут появляться вследствие предыдущей беременности (под влиянием HLA-антигенов мужа), перенесенных переливаний крови или произведенных ранее трансплантаций. Выявление этих антител имеет большое значение, так как некоторые из них могут обусловливать немедленное отторжение трансплантата.
Пересадка почки.
Неудивительно, что в проблеме трансплантации органов особое внимание уделяется почке. Почки – парный орган, и одну из них можно удалить у живого донора, не вызывая у него хронических нарушений почечной функции
Кроме того, к почке обычно подходит одна артерия, а кровь от нее оттекает по одной вене, что значительно упрощает методику восстановления ее кровоснабжения у реципиента. Мочеточник, по которому оттекает образующаяся в почке моча, можно тем или иным способом подсоединить к мочевому пузырю реципиента.
Впервые пересадку почки у животных осуществил в 1902 австрийский исследователь Э.Ульман. Значительный вклад в проблему трансплантации почки и сшивания кровеносных сосудов внес затем А.Каррель, работавший в Рокфеллеровском институте медицинских исследований (в настоящее время – Рокфеллеровский университет) в Нью-Йорке. В 1905 Каррель, совместно со своим сотрудником К.К.Гатри, опубликовал важнейшую работу, касающуюся гетеротопной и ортотопной (т.е. в необычное и обычное место) трансплантации почки у собаки. Ученые США и Европы продолжали экспериментировать на животных, но серьезные попытки пересадить почку человеку начались лишь с 1950. В это время группа врачей в Бостоне в больнице П.Б.Брайама провела ряд трансплантаций почки, что вызвало значительный интерес во всем мире и положило реальное начало пересадке органов у человека. Почти одновременно группа парижских врачей и чуть позднее хирурги в других странах также приступили к пересадке почки человеку. Хотя в то время реципиенты не получали средств, подавляющих реакцию отторжения, один из них жил после пересадки почти 6 месяцев. При этих первых операциях почку пересаживали на бедро (гетеротопная трансплантация), но затем были разработаны способы трансплантация в более естественное для нее место – в полость таза. Эта методика общепринята и сегодня.
В 1954 в больнице Брайама впервые пересадили почку от однояйцового близнеца. В 1959 там же осуществили пересадку почки от разнояйцового близнеца и впервые успешно воздействовали препаратами на реакцию отторжения, показав, что начавшаяся реакция не является необратимой. В том же 1959 был применен новый подход. Обнаружилось, что ряд средств, блокирующих клеточный метаболизм и получивших название антиметаболитов (в частности, азатиоприн), обладают мощным действием, подавляющим иммунный ответ. Специалисты в области пересадки тканей, особенно почек, быстро воспользовались этими данными, что и ознаменовало начало эры иммунодепрессантов в трансплантологии.
Применяя иммунодепрессивные средства, многие клиники достигли значительных успехов в продлении функции пересаженной человеку почки, и в 1987, например, только в США было произведено почти 9000 таких пересадок, а в мире – гораздо больше. Примерно в четверти проводимых в настоящее время трансплантаций почки донорами являются живые близкие родственники больного, добровольно отдающие одну свою почку. В остальных случаях используют почку у недавно умерших людей, хотя изредка и тех, кому по каким-то причинам показано ее удаление, или же у добровольцев, не являющихся родственниками реципиента.
Кратковременный положительный результат пересадки почки обычно наблюдается более чем у 75% больных, которым эта операция проводится в связи с необратимой утратой почечной функции. Столь высокий результат достигается благодаря типированию тканей и использованию комбинаций иммунодепрессивных средств, особенно циклоспорина и глюкокортикоидов. Успех теперь оценивают по длительности (год или несколько лет) выживания реципиента или функционирования трансплантата. Хотя многие больные живут и остаются здоровыми более 10 лет после пересадки почки, точный срок сохранения жизнеспособности трансплантата неизвестен. Не менее года после пересадки в настоящее время выживает более 90% больных. Жизнеспособность трансплантата зависит от того, у кого была взята почка: если у идентичного по HLA-антигенам родственника, вероятность приживления и функционирования трансплантата составляет 95%; если у живого родственника с полуидентичным (совпадает один гаплотип) набором HLA-антигенов, то вероятность приживления 80–90%; если же используют трупную почку, эта вероятность снижается до 75–85%. В настоящее время производят и повторные пересадки почки, но вероятность сохранения функции трансплантата в этих случаях ниже, чем при первой операции.
Что изменится с принятием нового закона о донорстве?
Главное нововведение – появится регистр волеизъявлений. Подобные регистры доноров и реципиентов существуют во всех странах. Предполагается, что регистр будет в электронном виде. В «Федеральный регистр донорских органов и пациентов-реципиентов» будет входить подрегистр, включающий волеизъявления граждан. Волеизъявление – это желание или нежелание человека стать донором после смерти. Оно не предусматривает какой-то конфиденциальной информации о параметрах его здоровья.
Кстати, согласие на донорство не означает, что органы человека обязательно будут использованы. Дать согласие сможет любой человек, вне зависимости от возраста и состояния здоровья. А вот станет ли донором человек, изъявивший согласие, будут решать врачи, если у этого человека будет констатирована смерть мозга. Предполагается, что регистр волеизъявлений будет давать человеку возможность менять свое решение.
Если согласия человека в регистре нет, а смерть мозга у него констатирована, врачи должны будут получить согласие у родственников. Без такого согласия изъятие органов будет невозможно.
Проблемы «черной» трансплантологии
Усиливают эти опасения и слишком уж явное несоответствие в доходах врачей США и ЕС с их российскими коллегами.
Вышеизложенное — отнюдь не призыв немедленно и любой ценой вводить в российских больницах американские зарплаты. Тем более, что «ценой» такой роскоши стала настолько дорогая медицина, что в США несколько десятков миллионов человек не могут пользоваться ее услугами.
Тем не менее, американскому эскулапу просто не имеет даже чисто экономического смысла реагировать на посулы «благодарности» за нужное заключение о наступлении смерти потенциального донора. Потому что в случае огласки он потеряет как минимум высокооплачиваемую работу.
А вот всегда ли такую стойкость смогут проявить российские врачи с их зарплатами? Тем более, моральный кодекс, моральные принципы у всех разные.
Так что, при всем уважении к озабоченности сенатором Беляковым проблемой низкого уровня трансплантаций в России, его инициатива ввести разрешающие донорство отметки на документах сама по себе вряд ли улучшит ситуацию. Для этого нужно успешно решать куда более серьезные проблемы.
Встройте «Правду.Ру» в свой информационный поток, если хотите получать оперативные комментарии и новости:
Подпишитесь на наш канал в или в
Добавьте «Правду.Ру» в свои источники в Яндекс.Новости или
Также будем рады вам в наших сообществах во
Поведение после процедуры
После процедуры нужно быть максимально осторожными. К своему здоровью нужно относиться бережно и придерживаться всех советов врача. Все это считается основными правилами после проведения процедуры, с помощью которых шансы на успешное закрепление и успешное вынашивание плода значительно возрастают.
Лечащий врач на консультации даст пациентке следующие рекомендации:
После процедуры очень важно избегать физической активности, а также отказаться от выполнения домашних дел, нужен полный покой;
Женщина не должна поднимать тяжести, так как это может повлиять на отторжение или перемещение зародыша.
Женщине необходимо воздержание от половой жизни, обычно это занимает 14 дней или несколько месяцев. Срок сможет определить только врач, он будет смотреть на то, как развивается плод и какие показатели риска выкидыша.
Наблюдать за показателями базальной температуры после проведения процедуры.
Нужно избегать стрессовых и тревожных ситуаций.
Уменьшить время за компьютером, отказаться от вождения автомобиля.
Воздержаться от алкогольных напитков и курения.
Не контактировать с больными ОРВИ.
Не принимать горячие ванны.
Прогуливаться на улице.
Беременность после пересадки эмбриона
Почему могут не прижиться эмбрионы?
На самом деле матка может расценить зародыш как инородное тело, от которого в дальнейшем избавиться по многочисленным причинам. К таким причинам относят:
- Миома матки.
- Перенесенный аборт.
- Проблемы с толщиной эндометрия.
- Недостаток прогестерона.
- Генетические отклонения эмбриона.
Препятствовать успешному проведению процедуры может излишний вес, женщины старше 45 лет, проблемы с работой иммунной системы. Когда зародыш не приживается, то у женщины начинается обычная менструация.
Даже если процедура пройдет хорошо, то это вовсе не означает, что получиться доносить плод до срока. Чтобы не произошел выкидыш, после того, как эмбрионы будут перенесены при ЭКО потребуется прогестероновая поддержка. Она делается с момента взятия яйцеклеток и до 14 недель беременности. Только медик может рассчитать необходимую дозировку препарата, все это делается с учетом индивидуальных особенностей.
Зачастую прием медикаментов прогестерона нужно закончить ближе к 14-15 неделе, однако когда уровень выкидыша высок, то принимать придется дольше.
Зачастую используют следующие средства:
- Дюфастон – средство, которое нужно каждый день употреблять внутрь;
- Утрожестан – капсулы или ампулы для введения во влагалище, содержащие в своем составе прогестерон, полученный из природного сырья;
- Кранон – гель, который предназначен для введения во влагалище;
- Лютеин – выпускается в таблетках или свечах для введения во влагалище.
Селезенка
Доктор Ониску говорит, что селезенка — это немного другой случай, так как это «орган, который фильтрует, ремонтирует и сохраняет красные кровяные клетки». Но при этом, по его словам, селезенка также не является необходимой для поддержания жизни, так что к ней применим тот же принцип.
После удаления селезенки пациент должен всю жизнь принимать антибиотики — но, опять же, все дело в балансе и в том, что более эффективно для пациента.
«Удаление и антибиотики — это меньший риск, чем перенести операцию по пересадке и до конца жизни принимать медикаменты, чтобы избежать отторжения», — уверяет Мейсон.
Будущее трансплантации
Image caption
Трансплантология не стоит на месте
Основное внимание всегда будет уделяться тем частям тела, которые поддерживают жизнь, однако, говорит доктор Ониску, «органы пересаживают по какой-то причине, это должно удовлетворять нужду пациента». «Вот почему мы, к примеру, делаем пересадку матки, — объясняет он
— Жить без этого органа можно, но пациентка может почувствовать, что не выполнит предназначение своей жизни, если у неё не будет детей. А пересадка матки удовлетворит нужду этой конкретной пациентки»
«Вот почему мы, к примеру, делаем пересадку матки, — объясняет он. — Жить без этого органа можно, но пациентка может почувствовать, что не выполнит предназначение своей жизни, если у неё не будет детей. А пересадка матки удовлетворит нужду этой конкретной пациентки».
Врачи уверены, что в будущем пациентам можно будет помогать не только при помощи традиционных операций по пересадке органов — вроде печени, сердца или легкого, — но и за счет регенерации и трансплантации клеток.
«Идеальный пример — пересадка клеток островков Лангерганса для лечения диабета, — говорит доктор Ониску, имея в виду крохотные скопления клеток, которые выделяют инсулин. — Для решения проблемы мы пересаживаем клетки из поджелудочной железы, а не всю железу целиком».
Image caption
Пересадка стволовых клеток может стать альтернативой пересадке органов
По мере того как растет спрос, медики изучают более сложные стратегии лечения, выходящие за пределы пересадки органов и клеточной терапии — и трансплантация все чаще дополняется регенеративной медициной, новыми технологиями и биоинженерией.
Ониску говорит: «Мы изучаем искусственные органы, то есть органы, которые восстанавливаются при помощи стволовых клеток, и, вероятно, даже органы, выращенные в иной среде, — ксенотранспланты». Так называются донорские органы или ткани, имеющие животное происхождение, а также человеческие органы, выращенный в теле животного для последующей пересадки людям.
История развития трансплантологии
Отправной точкой и началом возникновения науки о пересадке органов стало проведение первого переливания крови. После него развитие этой отрасли медицины проходило в два этапа.
Хирургический этап
Джозеф Мюррей – хирург, совершивший первую успешную пересадку почки
В этот период лечение состояло в удалении больного органа или его тканей способом хирургического вмешательства. Еще в древние времена лекари занимались «хирургией»: с помощью золотых и серебряных пластинок исправляли дефекты костей. Для этой цели использовалась также кокосовую скорлупу.
Хоть решения проблем пересадки были фактически нерешаемыми, попытки осуществить ее продолжались.
Так еще в XVII столетии во Франции Амбруаз Паре смог вживить принцессе здоровый зуб ее горничной. Пересадку костной ткани проводить не удавалось: организм отторгал ее как чужеродное тело. В остальных случаях она рассасывалась, не прижившись.
Биолого-хирургический этап
С течением времени ситуация менялась. Следующий период истории развития трансплантологии связан с возникновением более совершенных хирургических техник. Удаляя часть тела, утратившую функциональность, ученые заменяли ее здоровым органом. Впервые в ходе эксперимента для трансплантации была выбрана почка.
Параллельно в середине XX столетия появились новые подходы в области реаниматологии и в СССР. Ученые начали постигать новые методы трансплантологии:
- Был разработан автожектор для искусственной циркуляции крови. Созданный учеными Брюхоненко и Чечулиным аппарат запускает кровоток с помощью механизма, состоящего из двух насосов. Один из них подает кровь к артериям, другой перекачивает ее в венозные сосуды. К системе подключают насыщающий кровь кислородом оксигенатор и авторегулятор температуры тела.
- Проводились исследования, связанные с поиском материала для трансплантации. Результатом стало использование крови умершего, которая спасла жизнь больного при существенной кровопотере. Идея переливания крови трупа принадлежит профессору В.Н. Шамову (1928 год). Суть открытия – в подтверждении факта ее пригодности в течение 20-22 часов после наступления смерти.
- Пересадкой трупной почки занялся Вороной Ю.Ю. в 1934 г. Но из-за ее дефекта женщине, отправившейся парами ртути, выжить не удалось. К 1950 году попытки трансплантировать парный орган закончились неудачно.
Также велась работа в Европе: операцию по пересадке почки у козы провел хирург из Вены Э. Ульман еще в начале ХХ века. Событие вызвало волну возмущений со стороны противников и положительные отклики приверженцев.
Консервация органов.
Влюбом жизненно важном органе, предназначенном для пересадки, если он надолго лишен крови и кислорода, возникают необратимые изменения, которые не позволяют его использовать. Для сердца этот период измеряется минутами, для почки – часами
На разработку способов сохранения этих органов после их извлечения из организма донора тратятся огромные усилия. Ограниченного, но обнадеживающего успеха удается добиться путем охлаждения органов, снабжения их кислородом под давлением или перфузии охлажденными буферными растворами, консервирующими ткани. Почку, например, можно сохранять в таких условиях вне организма несколько дней.
Консервация органов увеличивает время, отпущенное на подбор реципиента путем проведения проб на совместимость, и обеспечивает пригодность органа. В рамках существующих в настоящее время региональных, национальных и даже международных программ производятся заготовка и распределение трупных органов, что позволяет их оптимально использовать. Тем не менее органов для пересадки не хватает. Можно надеяться, что, когда общество лучше осознает потребность в таких органах, их нехватка уменьшится и пересадки можно будет осуществлять быстрее и эффективнее.
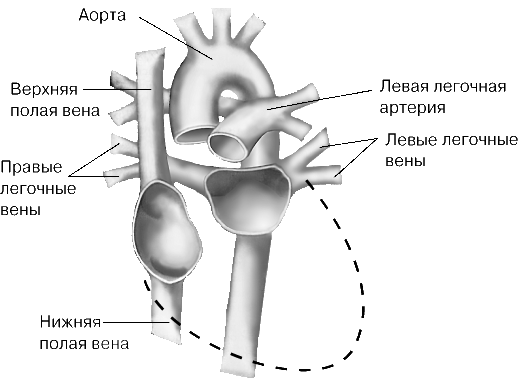
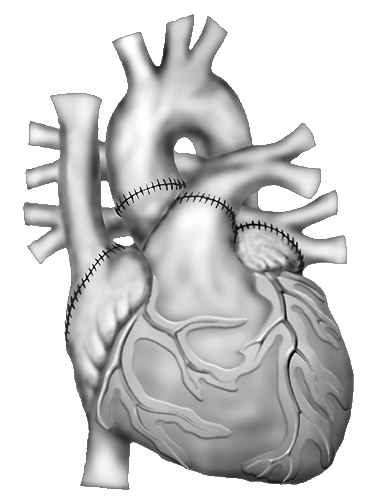
История трансплантации органов
История пересадки органов связаны с трудностями: попытки успешно повторить хирургическое вмешательство уже на человеческом организме не давали результата в течение нескольких десятилетий.
Трансплантация почки
И только по истечению 50 лет в 1991 году операция увенчалась успехом. Благодаря мастерству американских ученых мужчина с донорской почкой брата-близнеца прожил 20 с лишним лет. Хирург, проводивший трансплантацию, Дж. Мюррей был награжден Нобелевской премией.
Трансплантация печени
Томас Старлз вошел в историю трансплантологии, как первый человек, который провел пересадку печени.
После опытов на собаках (1963 год) хирург Томас Старзл провел пересадку этого одиночного органа. Но добиться ожидаемого результата не удалось, ровно как и при последующих попытках. Тщетные действия не были эффективными, так как препараты, угнетающие иммунитет, отсутствовали. Печень пересадили после появления прогрессивных технологий и новейшего медицинского оборудования.
Пересадка легких
Для пересаживания легких было сложно подобрать модель с нужными для эксперимента параметрами. Теоретически возможность трансплантации этого органа существовала и была продемонстрирована Демиховым В.П. в 1947 г. Практически за 20 лет ни одна из 61 операций не была проведена эффективно. Улучшение ситуации произошло после появления иммунодепрессанта циклоспорина: в 80-е годы прошлого века число успешных операций по приживлению легких возросло.
История трансплантации сердца
Возможность пересадки человеческого сердца также была доказана теоретически. После нескольких успешных экспериментов на животных хирурги попытались внедрить орган в грудную клетку человека:
| Период | Ученые, проводившие трансплантацию | Результат |
| 1905 год | Хирурги Коррель Гутри | Пересадка сердца собаки реципиента (проработало 2 часа) |
| С 1945 по 1948 годы | Трансплантолог Синицын А.П. | Опыт доказал право на существование пересадки (на примере лягушек) |
| 1955-й год | Хирург Демихов В.П. | Возможность пересадки в ходе эксперимента доказана. Разработка 24-х вариантов подключения к сосудистой системе |
| 1961 г. | Лоуер, Стофер и Шамуей | Публикация описания ортотопической пересадки сердца собаки |
| 1964 г. | Хирург по фамилии Горди (Миссисипи) | Пересадка пациенту сердца обезьяны (работало в течение 1 часа) |
|
1967-1968 |
Барнард Кристиан (Южная Африка, полуостров Кейптаун) | Первая пересадка человеческого сердца По истечению 3 недели после операции пациент умер от воспаления легких. Вторая успешная пересадка, после которой пациент прожил 2 года |
| 1968-1969
1978 |
Профессор Вишневский А.А. | Впервые в СССР осуществлена пересадка сердца. В мире проведены 100 хирургических вмешательств по пересадке сердца.
Медицина получила эффективный циклоспорин А, решивший проблему отторжения тканей |
С приходом 90-х годов специалисты в области трансплантологии значительно продвинулись в данном направлении. Новые знания о стволовых клетках сделали возможной также пересадку костного мозга, которая помогает восстанавливать кроветворные процессы.
Трансплантация сопряжена с этическими вопросами. Существуют сложные моральные аспекты: наличие серьезного риска для живого донора, необходимость согласия, причем осознанного и добровольного. Важна и конфиденциальность, которая обязательна при трансплантации. Но высокий уровень развития медицины дает шансы для продления жизни человека. Биологические законы отступают. История трансплантации органов является ярким тому доказательством.
Виды трансплантации органов и тканей
- Аутотрансплантация – это вид пересадки, когда реципиентом и донором одновременно является одно и то же лицо. К примеру, при сильных ожогах на теле пострадавшему пересаживают собственную кожу со здоровой части на пораженную. Тип аутотрансплантации больше всего наблюдается при проведении пластических операций. Хирургическим путем имплантируют части кожи, хрящи и сухожилия, мышечные ткани и кости конечностей и др.
- При ксенотрансплантации пересаживаются ткани от донора к организму другого человека. Это может быть и имплантация от животного к человеку, к примеру, использование кожи свиньи для пересадки.
- При гомотрансплантации пересаживаются ткани и органы от одного человека к другому человеку.
- Крайне редким видом трансплантации является изотрансплантация, когда выполняется пересадка между однояйцевыми близнецами, которые являются генетически идентичными организмами.
В зависимости от места пересадки органа или ткани, пересадка может называться:
- ортотопической – при ней орган донора пересаживают на его анатомическое место (сердце, легкие и печень);
- гетеротопической – орган донора пересаживается в другую область организма реципиента. Нежизнеспособный орган могут удалить, в некоторых случаях его оставляют. Такой вид трансплантации наблюдается при пересадке почки.
Чаще всего у живого человека пересаживаются такие органы, как сердце и почки, легкие и печень, селезенка, кишечник и его части, поджелудочная железа.
К объектам трансплантации можно отнести склеру и роговицу, сетчатку, глазное яблоко.
А если я не хочу быть донором после смерти?
Новый закон пока не принят, сейчас действует презумпция согласия. Но можно выразить и несогласие, федеральный закон «Об основах охраны здоровья граждан» (статья 47, пункты 6–10) это позволяет.
Там сказано, что совершеннолетний дееспособный гражданин может изъявить свое согласие или несогласие на донорство органов в устной форме, в присутствии свидетелей или в письменной форме, заверенной руководителем медицинской организации. При желании документ можно заверить нотариально – если человек хочет, чтобы документ имел юридическую силу. Информация о наличии волеизъявления гражданина вносится в его медицинскую документацию. Если волеизъявление отсутствует, право заявить о своем несогласии на изъятие органов и тканей из тела умершего для трансплантации имеют супруг (супруга), а при его (ее) отсутствии – один из близких родственников.