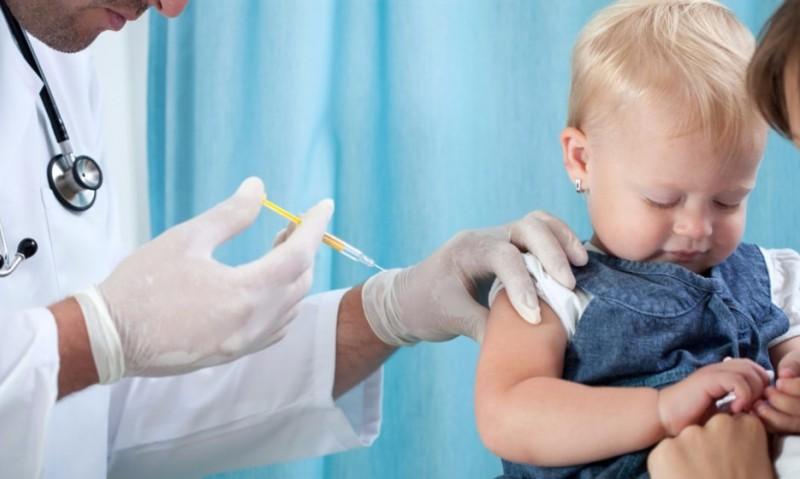
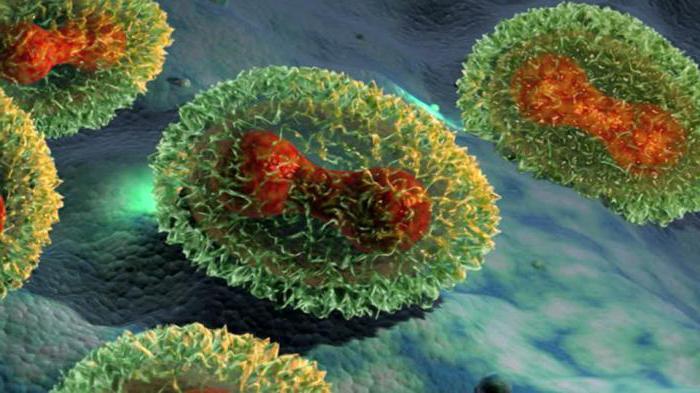
Гемагглютинин поверхностный антиген вируса гриппа ответствен за
Содержание:
- Как производят вакцины против гриппа?
- Ингибиторы нейраминидазы: список препаратов, инструкция по использованию
- Ученые придумали «крышку» на гемагглютинин – «абордажный крюк» вируса гриппа
- Вирус гриппа – смотрим врагу в лицо. Строение вируса гриппа (белки гемагглютинин и нейраминидаза)
- Новая цель в лечении рака мозга – фермент нейраминидаза
- Что обеспечивает высокую изменчивость вируса гриппа?
- Как гемагглютинин применяют в вакцинах?
Как производят вакцины против гриппа?
Есть разные технологии. Чаще всего, для того чтобы получить гемагглютинин, вирусы выращивают на куриных эмбрионах
В первую очередь важно понимать, от каких штаммов вируса нужна защита в текущем сезоне. Эксперты из Всемирной организации здравоохранения (ВОЗ) дважды в год проводят обзор мировой эпидемиологической ситуации и выпускают соответствующие рекомендации
Производители вакцин получают нужные штаммы из лабораторий ВОЗ.
Чтобы они стали более безопасными и лучше культивировались — их нужно правильно подготовить. Для этого штамм, против которого разрабатывают вакцину, «скрещивают» со стандартным лабораторным штаммом. Далее возбудителя нужно размножить, чтобы получить необходимое количество антигена. Для этого отлично подходят куриные яйца. Производитель их тщательно отбирает, ведь можно использовать только яйца абсолютно здоровых, не инфицированных другими возбудителями кур.
В специальной «зоне заражения» в яйцо через прокол вводят вирусы и инкубируют его в течение 48 часов. Затем из него извлекают жидкость с возбудителем и обрабатывают ее с помощью специального оборудования, чтобы удалить все лишние примеси, инактивировать вирус и очистить антигены.
Готовую вакцину нельзя сразу отправлять в больницы. Ее нужно протестировать с помощью реагентов, полученных из лаборатории ВОЗ. Обычно процесс занимает две недели. Сотрудники лаборатории проверяют, содержится ли в вакцине нужное количество антигена, нет ли посторонних примесей, насколько она безопасна, стерильна и так далее. Когда проверка окончена, препарат можно разливать по одноразовым шприцам. Каждый шприц повторно проверяют, чтобы убедиться, что он не поврежден, и в нем находится необходимая доза.
«Ранее использовались только трехвалентные вакцины против двух штаммов вируса гриппа A и одного B. Сейчас рекомендуется использовать четырехвалентные вакцины, в которые добавлен еще один штамм B. На каждый штамм должно приходиться по 15 мкг гемагглютинина на дозу. На российском рынке новую четырехвалентную вакцину «Ультрикс Квадри» в 2019 году представил холдинг «Нацимбио» Госкорпорации Ростех. Это первый в России препарат такого состава. На сегодняшний день в мире нет ничего совершеннее таких четырехвалентных вакцин – они защищают от гриппа эффективнее всего», – подчеркивает Олег Евтушенко.
Ингибиторы нейраминидазы: список препаратов, инструкция по использованию
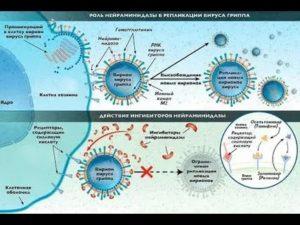
Международная система классификации препаратов лекарственного происхождения делит все медикаменты на группы. Основой для этого является фармакологическое действие веществ. Представленная статья расскажет вам об одной из таких групп. В нее входят ингибиторы нейраминидазы. Вы узнаете, какие действующие вещества являются их основой, а также ознакомитесь с их торговыми наименованиями.
Ингибиторы нейраминидазы
Перед тем как говорить о препаратах, необходимо дать характеристику данной фармакологической группе. Нейраминидаза – это своеобразный фермент.
Он присутствует на поверхности мембраны всех вирусов гриппа. После контакта с клеткой человеческого организма происходит выделение токсичных веществ.
Именно они и вызывают появление симптомов болезни: повышение температуры, слабость, головную боль и так далее.
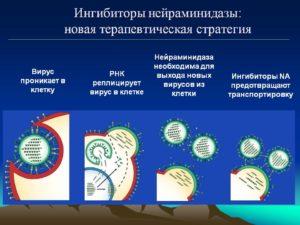
Ингибиторы нейраминидазы проникают внутрь вируса. Они подавляют активность патогенных микроорганизмов, предотвращая их последующее размножение и контакт со здоровыми клетками. Разработка таких препаратов началась еще в 1960-х годах. Первые произведенные средства позволили детально изучить их воздействие на вирусные инфекции.
Ингибиторы нейраминидазы: препараты и их действующие компоненты
Современная фармакология предлагает приобрести два основных препарата, которые могут характеризоваться подобным действием. Их торговые наименования «Тамифлю» и «Реленза». Оба средства применяются для профилактики и лечения гриппа разных штаммов. Продаются ингибиторы нейраминидазы только по назначению врача.
Также допускается использование медикаментов в условиях стационара по показаниям. Не рекомендуется принимать такие лекарства беременным женщинам и кормящим матерям. Противопоказанием к применению будет детский возраст до 5 лет.
Действующие вещества указанных препаратов отличаются названием и способом приема. Лекарство «Тамифлю» содержит в своем составе осельтамивир. Медикамент выпускается в виде капсул с сыпучим содержимым для внутреннего употребления. Препарат «Реленза» – это ингаляционное средство. Действующим компонентом является занамивир.
Способ применения препаратов
Каким способом используются ингибиторы нейраминидазы (гриппа)? Вы уже знаете, что оба медикамента прописываются врачом. Для приобретения препаратов вам потребуется соответствующий рецепт. Поэтому дозировку и продолжительность применения обычно выбирает специалист. Но в инструкции также имеется информация по этому поводу:
- Препарат «Тамифлю» у взрослых пациентов и детей после 12 лет используется дважды в сутки по одной таблетке. Продолжительность курса составляет 5 дней. Для малышей до 12 лет предпочтительно использовать суспензию в количестве 30-75 мг осельтамивира (в зависимости от массы тела) дважды в сутки.
- Лекарство «Реленза» поставляется ингаляционно. Инструкция рекомендует использовать 10 мг вещества (2 ингаляции) дважды в день. Продолжается терапия 5 суток. Для профилактики используется 10 мг препарата один раз в сутки на протяжении 10 дней.
Специалисты говорят, что ингибиторы нейраминидазы вирусов гриппа будут тем эффективнее, чем раньше начато лечение. Поэтому нужно при первых же симптомах обращаться к врачу.
Доктор назначит вам необходимые исследования, которые помогут определить дальнейшую тактику действий. Оба препарата эффективны в борьбе с вирусами гриппа (в том числе и мутировавшими).
В отличие от других противовирусных средств, ингибиторы нейраминидазы показывают высокую работоспособность. Уже через несколько часов после первого применения пациенту становится легче.
Важно, что «Реленза» и «Тамифлю» могут совмещаться с другими препаратами для лечения гриппа, его симптомов и осложнений. Кстати, лекарства имеют и побочные эффекты
Например, ингалятор «Реленза» может вызвать одышку и бронхоспазмы.
Редко возникает аллергия в виде отека. Средство «Тамифлю» принимается внутрь. Поэтому оно имеет больше негативных последствий: боль в животе, аллергия, обострение почечных и печеночных заболеваний, психоневрологические нарушения.
Подведем итоги
Ингибиторы нейраминидазы являются отличным средством в борьбе с вирусами гриппа. В период эпидемий они могут приниматься с целью профилактики. Но специалисты не рекомендуют использовать указанные медикаменты без особой нужды.
К тому же вы не можете приобрести лекарства по собственному желанию. Если фармацевт вам предлагает купить препарат «Тамифлю» или «Реленза» без рецепта, то знайте, что он может быть поддельным.
Применение таких медикаментов не только ухудшает течение болезни, но может оказаться опасным для жизни.
Ученые придумали «крышку» на гемагглютинин – «абордажный крюк» вируса гриппа
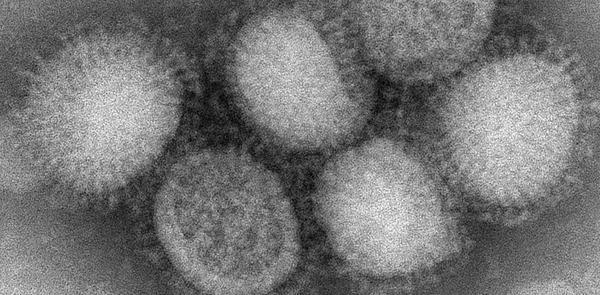
Частицы вируса гриппа N1H1 (свиной грипп), диаметр частиц 80—120 нм. Трансмиссионная электронная микроскопия
Гриппом болеет 3—5 миллионов человек в год, а 250—500 тысяч умирает от его осложнений; в основном это люди с ослабленной иммунной системой или пожилые. Геном вируса гриппа постоянно мутирует, и создать стабильно работающую вакцину против него не получается. Каждый год составляется новая композиция вакцин против гриппа в зависимости от того, какие штаммы преобладали в эпидемии предыдущего года. При этом, хотя так или иначе такие вакцины эффективны, специалистам не всегда удается точно «предугадать», какие штаммы вызовут эпидемию. Еще хуже дело обстоит с попытками лечить грипп: как известно, эта болезнь без лечения тянется неделю, а с лечением проходит всего за семь дней. Однако у вируса есть свои слабые места: поверхностные белки, обеспечивающие контакт с клеткой
Разработка лекарственных препаратов, способных предотвратить инфицирование клетки вирусом гриппа, основана на исследованиях молекулярных механизмов этого процесса, в котором принимают участие белки вируса – гемагглютинин и нейраминидаза, расположенные на поверхности оболочки вируса. Нейраминидаза в первую очередь необходима на стадии отделения созревших вирусных частиц от зараженной клетки, хотя участвует и во внедрении вируса в нее. Лекарства-ингибиторы нейраминидазы существуют; наверняка многие слышали или даже принимали такие препараты как тамифлю и реленза, которые активно рекламировались во время вспышки свиного гриппа в 2009 г. Еще одна группа препаратов, к которым относится всем известный ремантадин, блокирует тетрамер белка M2 – ионный канал, который служит насосом протонов и необходим для «раздевания» (разрушения оболочки и выхода наследственного материала) вируса гриппа в инфицированной клетке. Однако вирусы постепенно вырабатывают устойчивость к этим препаратам, так что ученые устремились к следующей цели – гемагглютинину.
Гемагглютинин нужен для проникновения вирусной частицы в клетку. Он присутствует на поверхности вируса в виде тримеров, то есть, комплексов из трех молекул. Верхняя часть этой молекулы, «голова», связывается с рецепторами мембраны клетки-мишени. В месте контакта образуется углубление, и вирус в итоге оказывается в клетке, сначала в полости эндоцитозного пузырька, из которого впоследствии высвобождается в цитоплазму.
Еще в 2011 г. исследователи из Вашингтонского университета в Сиэтле (США), создали белок, который связывается со «стволом» гемагглютинина, которым он крепится к вирусу, блокируя его способность заражать клетку, однако доступ к нужному участку часто затруднен из-за присутствия других вирусных белков, и эффективность препарата поэтому невысока.
Теперь ученые создали другой белок, который связывается с «головой» гемагглютинина. «Голова» более вариабельна, чем «ствол», но и на ней существуют высококонсервативные районы. Взяв за основу полученные с помощью рентгеноструктурного анализа данные о том, какие участки «головы» гемагглютинина связывают антитела, ученые разработали молекулу, «скопировав» участок антитела, которым оно связывается с гемагглютинином. Затем с помощью программы для предсказания структуры белков Rosetta они утроили этот участок, создав белок, состоящий из трех частей, которыми он тройной «крышкой» накрывает тример гемагглютинина, его «голову». Наконец, ученые наладили выпуск рекомбинантного белка, синтезировав кодирующий его ген и встроив его в геном кишечной палочки E. coli.
Затем исследователи провели несколько экспериментов, проверяя эффективность продукта. «Посадив» белок на нитроцеллюлозную мембрану, они получили «клейкую ленту» для вируса гриппа, удерживающую на себе различные его штаммы. Добавление белка в культуральную среду препятствовало заражению клеток вирусом, а его введение зараженным гриппом лабораторным мышам предотвращало у животных развитие заболевания.
Однако, пока это еще не лекарство. Не говоря о том, что полученную молекулу следует досконально проверить на безопасность для человека, новый белок все же не универсален. Он связывает вирусные частицы не всех штаммов, которые обычно поражают людей. Это означает, что в конечном итоге препарат, вероятно, будет представлять собой коктейль из похожих белков, связывающих разные варианты «головы» гемагглютинина, либо это будет сочетание с версиями, связывающими «ствол» гемагглютинина. И, возможно, на основе нового белка будет разработан экспресс-тест на вирус гриппа.
Вирус гриппа – смотрим врагу в лицо. Строение вируса гриппа (белки гемагглютинин и нейраминидаза)
Эпилог: статья больше для любознательных, желающих разбираться в обозначениях вируса: что значат буквы A, H1N1. Практической полезности для прагматиков, желающих начать профилактику или лечение, не несущая: расширяет кругозор, позволяет понять структуру вируса, проанализировать, понять с кем (а применительно для вирусов с чем) придется в итоге воевать. Для понимания механизмов распространения и борьбы с вирусом самое то.
Вирус – это микроскопическая частица (именно частица, а не организм, раньше даже считалось, что вирусы совсем и не живые организмы, а что-то вроде дерева или металла) состоящая из набора белков и нуклеиновых кислот (РНК или ДНК), способная инфицировать клетки живых организмов.
Возбудитель гриппа – это вирус, относящийся к семейству ортомиксовирусов, включает в себя три типа вирусов (типы A, B и C).
Все три типа значительно отличаются друг от друга по строению, поэтому при выработке защитных антител к одному типу (например, после болезни или вакцинации), можно спокойно заболеть другим типом вируса.
Кроме того, вирусы могут быстро мутировать в пределах своего типа (особенно типа A) и изменять структуру своих белков, за которые могут зацепиться защитные белки организма человека (антитела) и уничтожить вирус, что также затрудняет борьбу и меры профилактики против гриппа.
Именно этими факторами и объясняется, что каждый год огромное количество людей заболевает гриппом.
Теперь пройдемся по структуре вируса гриппа типа А и узнаем все эти непонятные буквы H или N которые все уже, думаю, слышали в новостях.
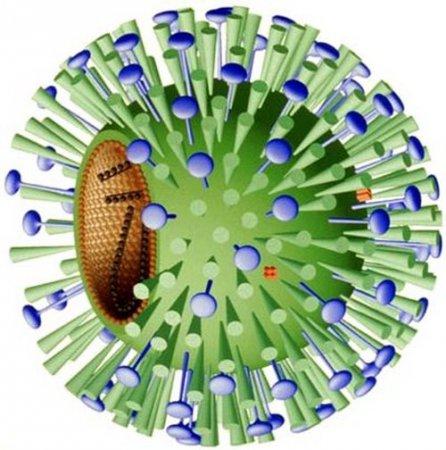
Вирус типа A включает в себя подтипы, которые различаются характеристиками белка гемагглютинина и фермента нейраминидазы.
Гемагглютинин (буковка H в подтипах вирусов от латинского названия Нemagglutinin) – поверхностный белок вируса гриппа, благодаря которому он может присоединяться к поверхности клетки хозяина, то есть некие такие клещи или щупальца, которыми вирус фиксируется на поверхности клеток. А надо отметить, что вирусы (любые, не только гриппа) могут существовать только, если фиксированы к клетке, ибо нет живого организма и вирус быстро погибает во внешней среде, особенно неблагоприятной для себя. Антитела именно к этому белку гемагглютинину и способствуют выработке иммунитета (барьера) против гриппа. Различают 15 антигенных подтипа этого белка: H1-H15
Нейраминизда (буква N, от Neuraminidase) – фермент, поверхностный антиген вируса, причем не только гриппа, а и многих других вирусов и бактерий. Поверхностный – это значит входит в состав оболочки вируса. Его роль заключается в разрушении рецепторов клеток организма к вирусу, благодаря чему вирус способен проникать к клеткам-мишеням (клеткам, где он внедряется, размножается, то есть проходит свой цикл), а также он облегчает высвобождение вновь образовавшихся вирусных частиц с поверхности зараженных клеток (размножение вируса). Для данного антигена гриппа характерны 9 подтипов: N1-N9
В результате мы имеем картину того, что вирус гриппа может иметь различную генетическую комбинацию, как в подтипах к гемагглютинину, так и в подтипах нейраминидазы, отсюда и вытекают различные типы вируса: H2N2, H3N2, H1N1 А учитывая еще разнородность и изменчивость структуры белка гемагглютинина, то комбинаций можно насоставлять на многие миллионы.
Что характерно, циркулирующий сейчас (будем верить вирусологам) вирус гриппа H1N1 это такой первенец, с которого начались последующие мутации набора белков и антигенов, произошло это в 1957 году, когда вирус типа H1N1 перешел в H2N2.
Вирусы гриппа типов B и C имеют меньше вариантов антигенов H и N и поэтому (возможно, что и пока) их на подтипы не делят.
Итог. Пытался написать это раздел максимально понятно, человеческим языком, если что-то конкретно не поняли, спрашивайте – поменяю, перепишу. Главное тут понять два момента:
1) вирус гриппа очень изменчив, по изменчивости он сравним с тем же вирусом иммунодефицита человека (ВИЧ/СПИД), который меняется в тех же пропорциях, что и вирус гриппа и поэтому лекарства доказанного и стопроцентно эффективного от него не найдено, также как и от вируса гриппа
2) теперь должны быть понятнее незнакомые до этого обозначения номенклатуры вируса гриппа, в частности почему новомодный свиной грипп называют вирусом А (тип вируса), H1N1 – набор гемагглютинина и нейраминидазы.
Новая цель в лечении рака мозга – фермент нейраминидаза
Фермент нейраминидаза находится в избыточном количестве в клетках глиобластомы, форме рака мозга
Появилась новая мишень для разработки селективных методов лечения рака мозга – фермент нейраминидаза. 22.08.2014 г. Недавно ученые разработали новые соединения, которые нацелены на лечение рака мозга.
Они синтезировал первый в своем роде ингибитор, который предотвращает активность фермента нейраминидазы.
Хотя вирусы гриппа используют эти ферменты с тем же механизмом как часть процесса инфицирования, клетки человека используют свои собственные формы фермента во многих биологических процессах.
Фермент нейраминидаза в клетках рака мозга
Ученые на пороге развития новых и более избирательных видов лечения рака. Исследователи разработали соединение, целью которого является фермент нейраминидаза, который избыточно экспрессируется в некоторых видах рака. Они проверили эффективность нового соединения в клетках рака головного мозга.
Ученые синтезировал первый в своем роде ингибитор, который предотвращает активность фермента нейраминидазы.
Хотя вирусы гриппа используют ферменты с тем же механизмом как часть процесса инфекции, клетки человека используют свои собственные формы фермента во многих биологических процессах.
Фермент нейраминидаза находится в избыточном количестве в клетках глиобластомы, форме рака мозга.
Новое соединение для лечения рака мозга
В новом исследовании ученые испытали селективный ингибитор фермента нейраминидазы и обнаружили, что стволовые раковые клетки глиобластомы (присутствуют в опухоли и стимулируют рост рака) превратились в нормальные клетки. Новое соединение также останавливало рост уже имеющихся раковых клеток, что имеет важное значение для лечения рака. Эти выводы показывают, что новый ингибитор фермента нейраминидазы может работать терапевтически и должен открыть двери для будущих исследований
Эти выводы показывают, что новый ингибитор фермента нейраминидазы может работать терапевтически и должен открыть двери для будущих исследований.
Он пока еще не является препаратом, но устанавливает новую цель, поэтому может быть применен для создания новых, более селективных препаратов.
Ингибитор фермента нейраминидазы – это еще не препарат
То, что это новое соединение может успешно подавлять фермент нейраминидазу в раковых клетках – это только первый шаг в определении его потенциала в качестве лечения.
Пока это соединение не может быть применено в качестве лекарственного средства, поскольку оно не создавалось для прохождения через гематоэнцефалический барьер.
В исследовании ученые использовали это соединение в очень высоких концентрациях.
Исследование также показывает, насколько важны углеводы в функционировании клеток. Хотя большинство из нас считает, что глюкоза (сахар в крови) – это единственный важный сахар в биологии, это все-таки не так. Существует целая область исследований – гликобиология, которая стремится понять функции сложных структур углеводов в клетках.
Углеводные структуры покрывают поверхность клеток, а также влияют на то, как клетки взаимодействуют друг с другом и с другими патогенами. Углеводы на поверхности клетки определяют, как она будет взаимодействует с другими клетками, поэтому они важны в развитии рака и других заболеваний.
Поскольку ученые могут создавать новые соединения, которые изменяют эти структуры, то могут влиять на эти взаимодействия. Ученые уже на протяжении десятилетий знают о том, что обнаруженные на раковых клетках углеводы очень сильно отличаются от таковых в нормальных клетках. Например, многие виды рака имеют разное количество конкретных остатков сиаловой кислоты.
Поиск новых целевых ферментов имеет важное значение для лечения рака, а это исследование показало, что можно селективно воздействовать на фермент нейраминидазу. Хотя было много работ, направленных на фермент нейраминидазу в вирусах, ученые создали ингибиторы ферментов человека. Сложность в клетках человека состоит в том, что существует четыре различных изофермента
Целью ингибитора нейраминидазы должен быть только один изофермент
Хотя было много работ, направленных на фермент нейраминидазу в вирусах, ученые создали ингибиторы ферментов человека. Сложность в клетках человека состоит в том, что существует четыре различных изофермента. Целью ингибитора нейраминидазы должен быть только один изофермент.
Что обеспечивает высокую изменчивость вируса гриппа?
Известно, что за это отвечают два процесса: антигенный дрейф и антигенный сдвиг.
В виду изменчивости, заложенной механизмом эволюции, фермент, синтезирующий вирусную РНК, не имеет защиты от неизбежных ошибок, из-за чего, в свою очередь, у одного штамма вируса возникают точечные мутации генов гемагглютинина и нейраминидазы . Можно сказать, что эти мутации возникают непрерывно, но каждая следующая не сильно отличается от предыдущей. При этом, именно из-за непрерывности этого процесса, эти мутации накапливаются в таком огромном количестве, что препятствуют распознаванию вируса иммунной системой, а это влечёт за собой необходимость периодических изменений состава противогриппозных вакцин в соответствии с прогнозами о преобладающих штаммах возбудителя в следующем эпидемическом сезоне. Помимо того, что антигенный дрейф присущ всем типам вируса гриппа, он встречается и у многих других вирусов. При этом вирус В мутирует в разы медленнее, чем вирус А, но быстрее, чем вирус С.
Гораздо более опасное свойство вируса гриппа. Плюсом, если вообще можно так выразится, можно назвать лишь то, что это свойство является особенностью только гриппа А. Заключается это свойство в способности вируса поражать множество видов животных, а также большим разнообразием гемагглютинина и нейраминидазы. Так, вирусы В и С содержат по одному типу этих гликопротеинов, которые внутри вида отличаются лишь относительно небольшим числом точечных мутаций, что существенно упрощает поиск вакцин. У вируса А на сегодняшний день известно 18 типов гемагглютинина и 11 типов нейраминидазы. Именно в соответствии с ними штаммы этого возбудителя имеют дополнительную маркировку, например, А/H1N1, А/H3N2 и т. д. Сродство вируса к разным видам птиц и зверей, из-за чего они становятся его разносчиками, зависит от конкретного типа этих антигенов. Но не стоит забывать, что, теоретически, любая разновидность вируса представляет опасность для всех подверженных гриппу видов. Более вирулентные и патогенные штаммы, с которыми иммунитет людей справляется очень плохо, возникают именно при антигенном сдвиге. Когда в одном организме встречаются вирусы с разными типами гемагглютинина и нейраминидазы, вирусные частицы в процессе сборки, из-за сегментированной РНК, могут «обмениваться» ими, что рано или поздно и приводит к появлению новых более агрессивных штаммов.
В результате этого процесса образовалось большинство разновидностей вируса А, вызывавших пандемии, например, «азиатского гриппа» в 1957 году или «гонконгского гриппа» в 1968 году. Недавняя пандемия 2009 года была вызвана обменом генами между человеческим, свиным и птичьим штаммами вируса. Происхождение возбудителя наиболее смертоносной пандемии гриппа в истории человечества — печально известной «испанки» 1918–20 годов, унесшей жизни, по разным оценкам, от 50 до 100 миллионов человек — менее понятно, но, вероятно, суть кроется всё в том же антигенном сдвиге. Как считает большинство учёных, исследовавших данный штамм, он мог появиться в результате антигенного сдвига при рекомбинации как минимум двух штаммов птичьего гриппа. Хотя есть версия и антигенного дрейфа, при котором «удачный» набор мутаций придал птичьему вирусу высокое сродство к человеческому организму.
Прошлогоднее исследование показало , что несмотря на все ухищрения возбудителя гриппа, с помощью которых он пытается обманывать «иммунитет», восприимчивость к определенным его штаммам, в том числе «незнакомым», зависит от типа вируса, которым человек переболел впервые в своей жизни. Суть кроется в том, что все разновидности гемагглютинина по аминокислотному составу делятся на две большие группы. Первая группа включает Н1, Н2, Н5, Н6, Н8, Н9, Н11-13 и Н16-18, а вторая — Н3, Н4, Н7, Н10, Н14 и Н15. К вирусам с антигенами той группы, с которой человек столкнулся впервые в жизни, у него развивается определенная степень устойчивости: заболевание либо не разовьется, либо будет протекать с минимальным риском летального исхода. На сегодня достоверно известно, что преобладание различных штаммов в структуре эпидемий меняется раз в несколько десятилетий, а значит чувствительность человека к той или иной разновидности вируса можно предсказать по году его рождения.
Как гемагглютинин применяют в вакцинах?
Гемагглютинин применяют в качестве антигена, для того чтобы «обучить» иммунитет и обеспечить защиту во время очередной эпидемии. Само по себе, без вирусной РНК, это вещество не заразно и не может вызвать инфекцию. Но оно вызывает иммунный ответ, и во время настоящей эпидемии организм встретит вирус уже во всеоружии.
В зависимости от того, насколько сильно разрушен вирус, противогриппозные вакцины делятся на три вида. Цельновирионные – содержат целые инактивированные вирусы; расщепленные (сплит-вакцины) – содержат отдельные фрагменты вирусов, а субъединичные – поверхностные и внутренние антигены вируса.
Побочные эффекты после введения вакцины возможны, но они бывают очень редко. У некоторых людей повышается температура, возникает легкое недомогание и боли в мышцах. Иногда болит место укола. Это происходит из-за того, что иммунная система реагирует на антигены и вызывает воспалительный процесс. Обычно симптомы сохраняются один день, потом проходят.