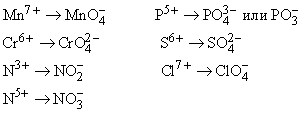Металлический водород
Содержание:
История исследований
В 1930-х годах британский ученый Джон Бернал предположил, что атомарный водород, состоящий из одного протона и одного электрона и представляющий собой полный аналог щелочных металлов, может оказаться стабильным при высоких давлениях. В 1935 году Юджин Вигнер и X. Б. Хантингтон провели соответствующие расчёты. Гипотеза Бернала нашла подтверждение — согласно полученным расчётам, молекулярный водород переходит в атомарную металлическую фазу при давлении около 250 тыс. атмосфер (25 ГПа) со значительным увеличением плотности. В дальнейшем оценка давления, требуемого для фазового перехода, была повышена, но условия перехода всё же считаются потенциально достижимыми. Предсказание свойств металлического водорода ведётся теоретически. Попытки получения, начатые в 1970-х годах, привели к возможным эпизодам водорода в 1996, 2008 и 2011 году, пока, наконец, в 2017 году профессор Айзек Сильвера и его коллега Ранга Диас не добились получения стабильного образца при давлении 5 млн атмосфер. Однако, камера где хранился образец, под давлением разрушилась и образец был потерян.
Экспериментальные попытки получения
Металлизация водорода ударным сжатием в 1996 году
В 1996 году Ливерморская национальная лаборатория сообщила, что в ходе исследований были созданы условия для металлизации водорода и получены первые свидетельства его возможного существования. Кратковременно (около 1 мс) было достигнуто давление более 100 ГПа (106{\displaystyle 10^{6}} атм.), температура порядка тысяч кельвинов при плотности вещества около 600 кг/м3. Поскольку предыдущие опыты по сжатию твердого водорода в ячейке с алмазными наковальнями до 250 ГПа не дали результата, целью эксперимента не было получение металлического водорода, а только изучение проводимости образца под давлением. Однако, по достижении 140 ГПа электрическое сопротивление практически исчезло. Ширина запрещенной зоны водорода под давлением составила 0.3 эВ, что оказалось сравнимо с тепловой энергией kT{\displaystyle kT}, соответствующей 3000 К и что свидетельствует о переходе «полупроводник — металл».
Исследования после 1996 года
Продолжались попытки перевести водород в металлическое состояние статическим сдавливанием при низких температурах. А. Руофф и Ч. Нараяна (Корнеллский университет, 1998), П. Лоувьер и Р. Летуле (2002) последовательно приближались к давлениям, наблюдаемым в центре Земли (324—345 ГПа), но все же не наблюдали фазового перехода.
Эксперименты 2008 года
Теоретически предсказанный максимум кривой плавления на фазовой диаграмме, указывающий на жидкую металлическую фазу водорода, был экспериментально обнаружен Ш. Деемьяд и И. Сильвера.
Группа М. Ереметца заявила о переходе силана в металлическое состояние и проявление сверхпроводимости, но результаты не были повторены.
Эксперименты 2011 года
В 2011 году было сообщено о наблюдении жидкой металлической фазы водорода и дейтерия при статическом давлении 260—300 ГПа.
, что вновь вызвало вопросы в научном сообществе.
Эксперименты 2015 года
26 июня 2015 году в журнале Science была опубликована статья, в которой описан успешный эксперимент группы исследователей из Сандийских национальных лабораторий (США) совместно с группой из Ростокского университета (Германия) по сжатию жидкого дейтерия (тяжёлого водорода) с помощью Z-Машины до состояния, которое проявляет .
Эксперименты 2016 года
В июле сообщалось, что физикам из Гарвардского университета удалось получить в лаборатории металлический водород. Они нагрели жидкий водород с помощью коротких вспышек лазера до температуры около 1900 градусов Цельсия и подвергли давлению в 1,1—1,7 мегабар.
Ожидается, что это вещество будет метастабильным, то есть при снятии давления останется металлом.
Эксперимент физиков помогает объяснить, какие процессы могут происходить в недрах газовых гигантов. Учёные предполагают, что в будущем металлический водород может быть использован в качестве ракетного топлива или как сверхпроводник, способный существовать при комнатной температуре.
Научное сообщество скептически отнеслось к данной новости, ожидая повторного эксперимента.
Применение водорода
Так как водород в 14 раз легче воздуха, то в былые времена им начиняли воздушные шары и дирижабли. Но после серии катастроф произошедших с дирижаблями конструкторам пришлось искать водороду замену (напомним, чистый водород – взрывоопасное вещество, и малейшей искры было достаточно, чтобы случился взрыв).

Взрыв дирижабля Гинденбург в 1937 году, причиной взрыва как раз и стало воспламенение водорода (вследствие короткого замыкания), на котором летал этот огромный дирижабль.
Поэтому для подобных летательных аппаратов вместо водорода стали использовать гелий, который также легче воздуха, получение гелия более трудоемкое, зато он не такой взрывоопасный как водород.
Тем не менее, водород весьма хорошо зарекомендовал себя в качестве одного из компонентов ракетного топлива. А автомобили, работающие на водородном топливе более экологичнее своих дизельных и бензиновых собратьев.
Также с помощью водорода производится очистка различных видов топлива, в особенности на основе нефти и нефтепродуктов.
Получение
В промышленности
Конверсия с водяным паром при 1000 °C:
-
- CH4+H2O ⇄ CO+3H2{\displaystyle {\mathsf {CH_{4}+H_{2}O\ \rightleftarrows {}\ CO+3H_{2}}}}
Пропускание паров воды над раскалённым коксом при температуре около 1000 °C:
-
- H2O+C ⇄ CO↑+H2↑{\displaystyle {\mathsf {H_{2}O+C\ \rightleftarrows {}\ CO\uparrow +H_{2}\uparrow }}}
Электролиз водных растворов солей:
-
- 2NaCl+2H2O → 2NaOH+Cl2↑+H2↑{\displaystyle {\mathsf {2NaCl+2H_{2}O\ {\xrightarrow {}}\ 2NaOH+Cl_{2}\uparrow +H_{2}\uparrow }}}
Электролиз водных растворов гидроксидов активных металлов (преимущественно, гидроксида калия) (англ.)
-
- 2H2O→4e−2H2↑+O2↑{\displaystyle {\ce {2H2O -> 2H2 ^ + O2 ^}}}
- Кроме того, существует промышленная технология электролиза химически чистой воды, без применения каких-либо добавок. Фактически, устройство представляет собой обратимый топливный элемент с твердой полимерной мембраной (англ.).
Каталитическое окисление кислородом:
-
- 2CH4+O2⇄ 2CO+4H2{\displaystyle {\mathsf {2CH_{4}+O_{2}\rightleftarrows {}\ 2CO+4H_{2}}}}
Крекинг и риформинг углеводородов в процессе переработки нефти.
В лаборатории
Действие разбавленных кислот на металлы. Для проведения такой реакции чаще всего используют цинк и разбавленную серную кислоту:
-
- Zn+H2SO4→ZnSO4+H2↑{\displaystyle {\mathsf {Zn+H_{2}SO_{4}\rightarrow ZnSO_{4}+H_{2}\uparrow }}}
Взаимодействие кальция с водой:
-
- Ca+2H2O→Ca(OH)2+H2↑{\displaystyle {\mathsf {Ca+2H_{2}O\rightarrow Ca(OH)_{2}+H_{2}\uparrow }}}
Гидролиз гидридов:
-
- NaH+H2O→NaOH+H2↑{\displaystyle {\mathsf {NaH+H_{2}O\rightarrow NaOH+H_{2}\uparrow }}}
Действие щелочей на цинк или алюминий:
-
- 2Al+2NaOH+6H2O→2NaAl(OH)4+3H2↑{\displaystyle {\mathsf {2Al+2NaOH+6H_{2}O\rightarrow 2Na+3H_{2}\uparrow }}}
-
- Zn+2KOH+2H2O→K2Zn(OH)4+H2↑{\displaystyle {\mathsf {Zn+2KOH+2H_{2}O\rightarrow K_{2}+H_{2}\uparrow }}}
С помощью электролиза. При электролизе водных растворов щелочей или кислот на катоде происходит выделение водорода, например:
-
- 2H3O++2e−→2H2O+H2↑{\displaystyle {\mathsf {2H_{3}O^{+}+2e^{-}\rightarrow 2H_{2}O+H_{2}\uparrow }}}
Очистка
В промышленности реализованы несколько способов очистки водорода из углерод-содержащего сырья (т. н. водородсодержащий газ — ВСГ).
- Низкотемпературная конденсация: ВСГ охлаждают до температур конденсации метана и этана, после чего водород отделяют ректификацией. Процесс ведут при температуре −158 °C и давлении 4 МПа. Чистота очищенного водорода составляет 93—94 % при его концентрации в исходном ВСГ до 40 %.
- Адсорбционное выделение на цеолитах: Настоящий метод на сегодняшний день наиболее распространен в мире. Метод достаточно гибок и может использоваться как для выделения водорода из ВСГ, так и для доочистки уже очищенного водорода. В первом случае процесс ведут при давлениях 3,0—3,5 МПа. Степень извлечения водорода составляет 80-85 % с чистотой 99 %. Во втором случае часто используют процесс «PSA» фирмы «Union Carbide». Он впервые был реализован в промышленности в 1978 году. На настоящий момент функционирует более 250 установок от 0,6 до 3,0 млн м3 Н2/сут. Образуется водород высокой чистоты 99,99 %.
- Абсорбционное выделение жидкими растворителями: Этот метод применяется редко, хотя водород получается высокой чистоты 99,9 %.
- Концентрирование водорода на мембранах: На лучших образцах метод позволяет получать водород чистотой 95-96 %, однако производительность таких установок невысока.
- Селективное поглощение водорода металлами: Метод основан на способности сплавов лантана с никелем, железа с титаном, циркония с никелем и других поглощать до 30 объёмов водорода.
Справка
Водород — первый элемент периодической системы элементов. Широко распространён в природе. Катион (и ядро) самого
распространённого изотопа водорода 1H — протон. Свойства ядра 1H позволяют широко использовать ЯМР-спектроскопию
в анализе органических веществ.
Некоторые изотопы водорода имеют собственные названия: 1 H — протий (Н),
2 H — дейтерий (D) и ³H — тритий (радиоактивен) (T).
Простое вещество водород — H 2 — лёгкий бесцветный газ. В смеси с воздухом или кислородом горюч и взрывоопасен. Нетоксичен. Растворим в
и ряде металлов:
,
,
,
.
История
Выделение горючего газа при взаимодействии кислот и металлов наблюдали в XVI и XVII веках на заре становления химии
как науки. Знаменитый английский физик и химик Г. Кавендиш в 1766 году исследовал этот газ и назвал его «горючим воздухом».
При сжигании «горючий воздух» давал воду, но приверженность Кавендиша теории флогистона помешала ему сделать правильные
выводы. Французский химик А. Лавуазье совместно с инженером Ж. Менье, используя специальные газометры, в 1783 г. осуществил
синтез воды, а затем и её анализ, разложив водяной пар раскалённым железом. Таким образом он установил, что «горючий воздух»
входит в состав воды и может быть из неё получен.
По распространённости в нашей Вселенной водород занимает первое место. На его долю приходится около 92% всех атомов
(8% составляют атомы гелия, доля всех остальных вместе взятых элементов — менее 0,1%). Таким образом, водород — основная
составная часть звёзд и межзвёздного газа. В условиях звёздных температур (например, температура поверхности Солнца ~ 6000 °С)
и межзвёздного пространства, пронизанного космическим излучением, этот элемент существует в виде отдельных атомов. Массовая
доля водорода в земной коре составляет — 1 % — это девятый по распространённости элемент. Однако его роль в природе определяется
не массой, а числом атомов, доля которых среди остальных элементов составляет 17% (второе место после кислорода, доля атомов
которого равна ~ 52%). Поэтому значение водорода в химических процессах, происходящих на Земле, почти так же велико, как и
кислорода. В отличие от кислорода, существующего на Земле и в связанном, и в свободном состояниях практически весь водород
на Земле находится в виде соединений; лишь в очень незначительном количестве водород в виде простого вещества содержится в
атмосфере (0,00005% по объёму).
Происхождение названия
Лавуазье дал водороду название hydrogène (от др.-греч. ὕδωρ — «вода» и γενναω — «рождаю») — «рождающий воду». Русское наименование
«водород» предложил химик М. Ф. Соловьев в 1824 году.
Меры предосторожности
Водород при смеси с воздухом образует взрывоопасную смесь — так называемый гремучий газ. Наибольшую взрывоопасность этот газ имеет при объёмном отношении водорода и кислорода 2:1, или водорода и воздуха приближённо 2:5, так как в воздухе кислорода содержится примерно 21 %. Также водород пожароопасен. Жидкий водород при попадании на кожу может вызвать сильное обморожение.
Считается, что взрывоопасные концентрации водорода с кислородом возникают от 4 % до 96 % объёмных. При смеси с воздухом от 4 % до 75 (74) % по объёму. Такие цифры фигурируют сейчас в большинстве справочников, и ими вполне можно пользоваться для ориентировочных оценок. Однако следует иметь в виду, что более поздние исследования (примерно конец 80-х) выявили, что водород в больших объёмах может быть взрывоопасен и при меньшей концентрации. Чем больше объём, тем меньшая концентрация водорода опасна.
Источник этой широко растиражированной ошибки в том, что взрывоопасность исследовалась в лабораториях на малых объёмах. Поскольку реакция водорода с кислородом — это цепная химическая реакция, которая проходит по свободнорадикальному механизму, «гибель» свободных радикалов на стенках (или, скажем, поверхности пылинок) критична для продолжения цепочки. В случаях, когда возможно создание «пограничных» концентраций в больших объёмах (помещения, ангары, цеха), следует иметь в виду, что реально взрывоопасная концентрация может отличаться от 4 % как в большую, так и в меньшую стороны.
Ракетное топливо
Жидкий водород является распространенным компонентом ракетного топлива, которое используется для реактивного ускорения ракет-носителей и космических аппаратов. В большинстве жидкостных ракетных двигателей на водороде, он сначала применяется для регенеративного охлаждения сопла и других частей двигателя, перед его смешиванием с окислителем и сжиганием для получения тяги. Используемые современные двигатели на компонентах H2/O2 потребляют переобогащенную водородом топливную смесь, что приводит к некоторому количеству несгоревшего водорода в выхлопе. Кроме увеличения удельного импульса двигателя за счет уменьшения молекулярного веса, это ещё сокращает эрозию сопла и камеры сгорания.
Такие препятствия использования ЖВ в других областях, как криогенная природа и малая плотность, являются также сдерживающим фактором для использования в данном случае. На 2009 год существует только одна ракета-носитель («Дельта-4»), которая целиком является водородной ракетой. В основном ЖВ используется либо на верхних ступенях ракет, либо на разгонных блоках, которые значительную часть работы по выводу полезной нагрузки в космос выполняют в вакууме. В качестве одной из мер по увеличению плотности этого вида топлива существуют предложения использования шугообразного водорода, то есть полузамерзшей формы ЖВ.
Водород с разными окислителями
Данные приводятся на основании таблиц, опубликованных в США в рамках проекта сбора термодинамических данных «JANAF» (англ. Joint Army Navy Air Force, «Сборник ВМС и ВВС армии США»), которые широко используются в этих целях. Изначально вычисления производились компанией «Рокетдайн». При этом делались предположения, что имеет место адиабатическое сгорание, изоэнтропийное расширение в одном направлении и имеет место смещение равновесного состояния. Кроме варианта использования водорода в качестве топлива, приводятся варианты с использованием водорода в качестве рабочего тела, что объясняется его небольшим молекулярным весом. Все данные рассчитаны для давления в камере сгорания («КС»), равного 68,05 атмосфер. Последняя строка таблицы содержит данные для газообразных водорода и кислорода.
| Оптимальное расширение от 68.05 атм до условий: | поверхности Земли (1 атм) | вакуума (0 атм, расширение сопла 40:1) | ||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Окислитель | Топливо | Комментарий | Ve | r | Tc | d | C* | Ve | r | Tc | d | C* |
| жO2 | H2 | распространено | 3816 | 4.13 | 2740 | 0.29 | 2416 | 4462 | 4.83 | 2978 | 0.32 | 2386 |
| H2-Be 49/51 | 4498 | 0.87 | 2558 | 0.23 | 2833 | 5295 | 0.91 | 2589 | 0.24 | 2850 | ||
| CH4/H2 92.6/7.4 | 3126 | 3.36 | 3245 | 0.71 | 1920 | 3719 | 3.63 | 3287 | 0.72 | 1897 | ||
| F2 | H2 | 4036 | 7.94 | 3689 | 0.46 | 2556 | 4697 | 9.74 | 3985 | 0.52 | 2530 | |
| H2-Li 65.2/34.0 | 4256 | 0.96 | 1830 | 0.19 | 2680 | |||||||
| H2-Li 60.7/39.3 | 5050 | 1.08 | 1974 | 0.21 | 2656 | |||||||
| OF2 | H2 | 4014 | 5.92 | 3311 | 0.39 | 2542 | 4679 | 7.37 | 3587 | 0.44 | 2499 | |
| F2/O2 30/70 | H2 | 3871 | 4.80 | 2954 | 0.32 | 2453 | 4520 | 5.70 | 3195 | 0.36 | 2417 | |
| O2 | H2 | 3997 | 3.29 | 2576 | — | 2550 | 4485 | 3.92 | 2862 | — | 2519 |
| В таблице использованы обозначения: | r | — массовое соотношение смеси «окислитель/топливо»; | |
| Ve | [м/сек] | — средняя скорость истечения газов; | |
| C* | [м/сек] | — характеристическая скорость; | |
| Tc | [°C] | — температура в КС; | |
| d | [г/см³] | — средняя плотность топлива и окислителя; |
при этом «Ve» является той же единицей, что и удельный импульс, но приведена к размерности скорости [Н*сек/кг], а «C*» вычисляется путём умножения давления в камере сгорания на коэффициент расширения площади сопла и последующего деления на массовый расход топлива и окислителя, что дает приращение скорости на единицу массы.
Получение
Основная статья: Производство водорода
См. также: Биотехнологическое получение водорода
В промышленности
Конверсия с водяным паром при 1000 °C:
-
- CH4+H2O ⇄ CO+3H2{\displaystyle {\mathsf {CH_{4}+H_{2}O\ \rightleftarrows {}\ CO+3H_{2}}}}
Пропускание паров воды над раскалённым коксом при температуре около 1000 °C:
-
- H2O+C ⇄ CO↑+H2↑{\displaystyle {\mathsf {H_{2}O+C\ \rightleftarrows {}\ CO\uparrow +H_{2}\uparrow }}}
Электролиз водных растворов солей:
-
- 2NaCl+2H2O → 2NaOH+Cl2↑+H2↑{\displaystyle {\mathsf {2NaCl+2H_{2}O\ {\xrightarrow {}}\ 2NaOH+Cl_{2}\uparrow +H_{2}\uparrow }}}
Электролиз водных растворов гидроксидов активных металлов (преимущественно, гидроксида калия) (англ.)
-
- 2H2O→4e−2H2↑+O2↑{\displaystyle {\ce {2H2O -> 2H2 ^ + O2 ^}}}
- Кроме того, существует промышленная технология электролиза химически чистой воды, без применения каких-либо добавок. Фактически, устройство представляет собой обратимый топливный элемент с твердой полимерной мембраной (англ.).
Каталитическое окисление кислородом:
-
- 2CH4+O2⇄ 2CO+4H2{\displaystyle {\mathsf {2CH_{4}+O_{2}\rightleftarrows {}\ 2CO+4H_{2}}}}
Крекинг и риформинг углеводородов в процессе переработки нефти.
В лаборатории
Действие разбавленных кислот на металлы. Для проведения такой реакции чаще всего используют цинк и разбавленную серную кислоту:
-
- Zn+H2SO4→ZnSO4+H2↑{\displaystyle {\mathsf {Zn+H_{2}SO_{4}\rightarrow ZnSO_{4}+H_{2}\uparrow }}}
Взаимодействие кальция с водой:
-
- Ca+2H2O→Ca(OH)2+H2↑{\displaystyle {\mathsf {Ca+2H_{2}O\rightarrow Ca(OH)_{2}+H_{2}\uparrow }}}
Гидролиз гидридов:
-
- NaH+H2O→NaOH+H2↑{\displaystyle {\mathsf {NaH+H_{2}O\rightarrow NaOH+H_{2}\uparrow }}}
Действие щелочей на цинк или алюминий:
-
- 2Al+2NaOH+6H2O→2NaAl(OH)4+3H2↑{\displaystyle {\mathsf {2Al+2NaOH+6H_{2}O\rightarrow 2Na+3H_{2}\uparrow }}}
-
- Zn+2KOH+2H2O→K2Zn(OH)4+H2↑{\displaystyle {\mathsf {Zn+2KOH+2H_{2}O\rightarrow K_{2}+H_{2}\uparrow }}}
С помощью электролиза. При электролизе водных растворов щелочей или кислот на катоде происходит выделение водорода, например:
-
- 2H3O++2e−→2H2O+H2↑{\displaystyle {\mathsf {2H_{3}O^{+}+2e^{-}\rightarrow 2H_{2}O+H_{2}\uparrow }}}
Очистка
В промышленности реализованы несколько способов очистки водорода из углерод-содержащего сырья (т. н. водородсодержащий газ — ВСГ).
- Низкотемпературная конденсация: ВСГ охлаждают до температур конденсации метана и этана, после чего водород отделяют ректификацией. Процесс ведут при температуре −158 °C и давлении 4 МПа. Чистота очищенного водорода составляет 93—94 % при его концентрации в исходном ВСГ до 40 %.
- Адсорбционное выделение на цеолитах: Настоящий метод на сегодняшний день наиболее распространен в мире. Метод достаточно гибок и может использоваться как для выделения водорода из ВСГ, так и для доочистки уже очищенного водорода. В первом случае процесс ведут при давлениях 3,0—3,5 МПа. Степень извлечения водорода составляет 80-85 % с чистотой 99 %. Во втором случае часто используют процесс «PSA» фирмы «Union Carbide». Он впервые был реализован в промышленности в 1978 году. На настоящий момент функционирует более 250 установок от 0,6 до 3,0 млн м3 Н2/сут. Образуется водород высокой чистоты 99,99 %.
- Абсорбционное выделение жидкими растворителями: Этот метод применяется редко, хотя водород получается высокой чистоты 99,9 %.
- Концентрирование водорода на мембранах: На лучших образцах метод позволяет получать водород чистотой 95-96 %, однако производительность таких установок невысока.
- Селективное поглощение водорода металлами: Метод основан на способности сплавов лантана с никелем, железа с титаном, циркония с никелем и других поглощать до 30 объёмов водорода.
Физические свойства
Эмиссионный спектр излучения атомов водорода на фоне сплошного спектра в видимой области
Эмиссионный спектр атомов водорода. Четыре видимые глазом спектральные линии серии Бальмера
Водород — самый лёгкий газ: он легче воздуха в 14,5 раз. Поэтому, например, мыльные пузыри, наполненные водородом, на воздухе стремятся вверх. Чем меньше масса молекул, тем выше их скорость при одной и той же температуре. Как самые лёгкие, молекулы водорода движутся быстрее молекул любого другого газа и тем самым быстрее могут передавать теплоту от одного тела к другому. Отсюда следует, что водород обладает самой высокой теплопроводностью среди газообразных веществ. Его теплопроводность примерно в 7 раз выше теплопроводности воздуха.
Молекула водорода двухатомна — Н2. При нормальных условиях это газ без цвета, запаха и вкуса. Плотность 0,08987 г/л (н. у.), температура кипения −252,76 °C, удельная теплота сгорания 120,9·106 Дж/кг, малорастворим в воде — 18,8 мл/л.
Водород хорошо растворим во многих металлах (Ni, Pt, Pd и др.), особенно в палладии (850 объёмов H2 на 1 объём Pd). С растворимостью водорода в металлах связана его способность диффундировать через них; диффузия через углеродистый сплав (например, сталь) иногда сопровождается разрушением сплава вследствие взаимодействия водорода с углеродом (так называемая декарбонизация). Практически не растворим в серебре.
Фазовая диаграмма водорода
Жидкий водород существует в очень узком интервале температур от −252,76 до −259,2 °C. Это бесцветная жидкость, очень лёгкая (плотность при −253 °C 0,0708 г/см³) и текучая (вязкость при −253 °C 13,8 сП). Критические параметры водорода очень низкие: температура −240,2 °C и давление 12,8 атм. Этим объясняются трудности при ожижении водорода.
В жидком состоянии равновесный водород состоит из 99,79 % пара-Н2, 0,21 % орто-Н2.
Твёрдый водород, температура плавления −259,2 °C, плотность 0,0807 г/см³ (при −262 °C) — снегоподобная масса, кристаллы гексагональной сингонии, пространственная группа P6/mmc, параметры ячейки a = 0,378 нм и c = 0,6167 нм.
В 1935 году Уингер и Хунтингтон высказали предположение о том, что при давлении свыше 250 тысяч атм водород может перейти в металлическое состояние. Получение этого вещества в устойчивом состоянии открывало очень заманчивые перспективы его применения — ведь это был бы сверхлёгкий металл, компонент лёгкого и энергоёмкого ракетного топлива. В 2014 году было установлено, что при давлении порядка 1,5—2,0 млн атм водород начинает поглощать инфракрасное излучение, а это означает, что электронные оболочки молекул водорода поляризуются. Возможно, при ещё более высоких давлениях водород превратится в металл. В 2017 году появилось сообщение о возможном экспериментальном наблюдении перехода водорода в металлическое состояние под высоким давлением.
Молекулярный водород существует в двух спиновых формах (модификациях): ортоводород и параводород.
Модификации немного различаются по физическим свойствам, оптическим спектрам, также по характеристикам рассеивания нейтронов. В молекуле ортоводорода o-H2 (т. пл. −259,10 °C, т. кип. −252,56 °C) спины ядер параллельны, а у параводорода p-H2 (т. пл. −259,32 °C, т. кип. −252,89 °C) — противоположно друг другу (антипараллельны). Равновесная смесь o-H2 и p-H2 при заданной температуре называется равновесный водород e-H2.
Равновесная мольная концентрация параводорода в смеси в зависимости от температуры
Разделить модификации водорода можно адсорбцией на активном угле при температуре жидкого азота. При очень низких температурах равновесие между ортоводородом и параводородом почти нацело сдвинуто в сторону параводорода, так как энергия пара-молекулы немного ниже энергии орто-молекулы. При 80 К соотношение модификаций приблизительно 1:1. Десорбированный с угля параводород при нагревании превращается в ортоводород с образованием равновесной смеси. При комнатной температуре равновесна смесь ортоводорода и параводорода в отношении около 75:25. Без катализатора взаимное превращение происходит относительно медленно, что даёт возможность изучить свойства обеих модификаций. В условиях разреженной межзвёздной среды характерное время перехода в равновесную смесь очень велико, вплоть до космологических.
Применение
Водород сегодня применяется во многих областях. Структура мирового потребления водорода представлена в следующей таблице
| Применение | Доля |
|---|---|
| Производство аммиака | 54 % |
| Нефтепереработка и химическая промышленность | 35 % |
| Производство электроники | 6 % |
| Металлургия и стекольная промышленность | 3 % |
| Пищевая промышленность | 2 % |
Химическая промышленность
Химическая промышленность — это крупнейший потребитель водорода. Около 50 % мирового выпуска водорода идёт на производство аммиака. Ещё около 8 % используется для производства метанола. Из аммиака производят пластмассы, удобрения, взрывчатые вещества и прочее. Метанол является основой для производства некоторых пластмасс.
Нефтеперерабатывающая промышленность
В нефтепереработке водород используется в процессах гидрокрекинга и гидроочистки, способствуя увеличению глубины переработки сырой нефти и повышению качества конечных продуктов. Для этих целей используется порядка 37 % всего производимого в мире водорода.
Пищевая и косметическая промышленность
При производстве саломаса (твердый жир, производимый из растительных масел). Саломас является основой для производства маргарина, косметических средств, мыла. Водород зарегистрирован в качестве пищевой добавки E949.
Химические лаборатории
Водород используется в химических лабораториях в качестве газа-носителя в газовой хроматографии. Такие лаборатории есть на многих предприятиях в пищевой, парфюмерной, металлургической и химической промышленности. Несмотря на горючесть водорода, его использование в такой роли считается достаточно безопасным, поскольку водород используется в незначительных количествах. Эффективность водорода как газа-носителя при этом лучше, чем у гелия, при существенно более низкой стоимости.
Авиационная промышленность
В настоящее время водород в авиации не используется. Когда-то дирижабли и воздушные шары наполняли водородом. Но в 30-х гг. XX в. произошло несколько катастроф, в ходе которых дирижабли взрывались и сгорали. В наше время дирижабли наполняют гелием, несмотря на его существенно более высокую стоимость.
Метеорология
Водород используется в метеорологии для заполнения оболочек метеозондов. Водород в этом качестве имеет преимущество перед гелием, так как он дешевле. Ещё более существенно, что водород вырабатывается прямо на метеостанции с помощью простого химического генератора или с помощью электролиза воды. Гелий же должен доставляться на метеостанцию в баллонах, что может быть затруднительно для удаленных мест.
Топливо
Водород используют в качестве ракетного топлива. Ввиду крайне узкого диапазона температур (менее 7 кельвинов), при котором водород остается жидкостью, на практике чаще используется смесь жидкой и твёрдой фаз (шугообразный водород).
Ведутся исследования по применению водорода как топлива для легковых и грузовых автомобилей, хотя здесь серьезную проблему представляет водородное охрупчивание сталей, не позволяющее напрямую переводить обычный ДВС на этот газ. Водород в ДВС меньше загрязняет окружающую среду локально (использование водорода в этом качестве затрудняет низкая эффективность его получения и сопряжённых дополнительных расходов на его сжатие, транспортировку), но так же, как и бензиновые/дизельные аналоги, потребляет и деградирует моторное масло и все остальные неэкологичные материалы, присущие двигателям внутреннего сгорания. В смысле экологии электромобили значительно лучше, перспективен также двигатель Стирлинга.[источник не указан 2116 дней]
В водородно-кислородных топливных элементах используется водород для непосредственного преобразования энергии химической реакции в электрическую.
Прочее
Атомарный водород используется для атомно-водородной сварки. Высокая теплопроводность водорода используется для заполнения сфер гирокомпасов и стеклянных колб филаментных LED-лампочек.
Водородные круги на полях.


«Ведьмин круг» — полоска более сочной и высокой травы по границе идеально ровной окружности — она особенно хорошо заметна на обычно сухих участках земли. Интенсивный рост растений в кольцах не связан с особенностями грунта или подземными источниками воды, но вполне объясним выходом водорода. Причём, проходя через плодородный слой почвы, газ обесцвечивает её. В интенсивных местах выхода первородного газа наблюдается проседание почвы и образование водоемов.

После долгой зимы газ скапливается под промерзшим слоем почвы и прорывается на поверхность, образуя кучи рыхлой Земли, похожие на муравейники, за которые их часто принимают!

Более значительные объёмы газов скапливаются под слоем вечной мерзлоты, образуя бугры пучения.

Бугры пучения на Ямале, и их дальнейшая взрывная эволюция.

Примечания
- ↑
- Севергин В. М. Пробирное искусство, или руководство к химическому испытанию металлических руд и других ископаемых тел. СПб.: Издание Имп. АН, 1801. C. 2.
- Н. Гринвуд, А. Эрншо. Химия элементов: в 2 томах. — БИНОМ. Лаборатория знаний, 2008. — Т. 1. — С. 11. — 607 с. — (Лучший зарубежный учебник). — ISBN 978-5-94774-373-9.
- Gribbin, John. Science. A History (1543-2001). — L.: Penguin Books, 2003. — 648 с. — ISBN 978-0-140-29741-6.
- ↑
- А.К.Мановян. Технология переработки природных энергоносителей. — Москва: Химия, КолосС, 2004. — 456 с. — ISBN 5-98109-004-9, 5-9532-0219-97.
- Неограническая химия. Том 2. Химия непереходных элементов / под ред. акад. Ю. Д. Третьякова. — Москва: Академия, 2004. — 368 с. — ISBN 5-7695-1436-1.
- ↑
- Züttel A., Borgschulte A., Schlapbach L. Hydrogen as a Future Energy Carrier. — Wiley-VCH Verlag GmbH & Co. KGaA, 2008. — ISBN 978-3-527-30817-0.
- Гресов А. И., Обжиров А. И., Яцук А. В. К вопросу водородоносности угольных бассейнов Дальнего востока/ Вестник КРАУНЦ. Науки о Земле. 2010, № 1, Выпуск 15. С. 19—32.
- ↑ Р. В. Радченко, А. С. Мокрушин, В. В. Тюльпа. Водород в энергетике. — Екатеринбург: Издательство Уральского университета, 2014. — С. 24. — 229 с. — ISBN 978-5-7996-1316-7.