Препараты на основе бактериофагов
Содержание:
Способы эксплуатации
Вирусы бактериофаги находят свое широкое применение в терапии антибактериального типа, которая служит альтернативой антибиотикам. Среди организмов, которые могут быть применимы, чаще всего выделяют: стрептококковых, стафилококковых, клебсиеллезных, коли, протейных, пиобактериофагов, полипротейновых и дизентерийных.
На территории РФ в медицинских целях зарегистрировано и применимо на практике тринадцать медикаментозных веществ, основанных на фагах. Как правило, такие способы борьбы с инфекциями применяются в том случае, когда традиционная форма лечения не приводит к значительным изменениям, что обуславливается слабой чувствительностью возбудителя к самому антибиотику или полному сопротивлению. На практике использование бактериофагов приводит к быстрому и качественному достижению желаемого успеха, но для этого необходимо присутствие биологической мембраны, укрытой слоем полисахаридов, сквозь которые антибиотикам проникнуть не удается.
Терапевтический тип применения представителей фагов не находит поддержания на Западе. Однако часто применяется для борьбы с бактериями, вызывающими пищевое отравление. Многолетние опыты по исследованию деятельности бактериофагов показывают нам, что наличие, например, дизентерийного фага в общем пространстве городов и сел обуславливает подвергание пространства профилактическим мерам.
Инженеры-генетики эксплуатируют бактериофагов, как векторы, при помощи которых осуществляется перенос участков ДНК. А также с их участием протекает передача геномной информации между взаимодействующими клетками бактерий.
Поскольку бактериофаги не инфицируют клетки человека, они используются в медицинской терапии для лечения бактериальных заболеваний.
Общие данные
Прежде чем рассмотреть представителей вирусов – бактериофагов, — ознакомимся с общими сведениями о данном царстве таксономической иерархии.
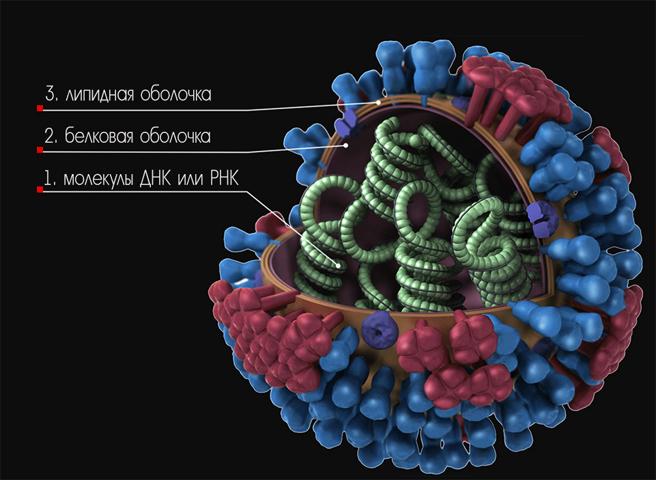
Вирусная частичка имеет мельчайшие размеры (20-300 нм) и симметричное структурирование. Строится из постоянно повторяющихся компонентов. Все организмы вирусной природы являются фрагментом РНК или ДНК, заключаются в особую оболочку из белка, называемую капсидом. Они не обладают способностью самостоятельно функционировать и поддерживать жизнедеятельность, находясь вне другой клетки. Проявление свойств живых существ им присуще лишь после внедрения в другой организм, при этом сам вирус будет использовать ресурсы захваченной им клетки для поддержания стабильности в собственном состоянии. Из этого следует, что данный домен таксономии представлен в виде паразитической, внутриклеточной формы жизни. Существуют вирусы, захватывающие участки мембран клетки, в которой они развивались и жили. Они образуют вокруг таких мест еще одну оболочку, покрывающую капсид.
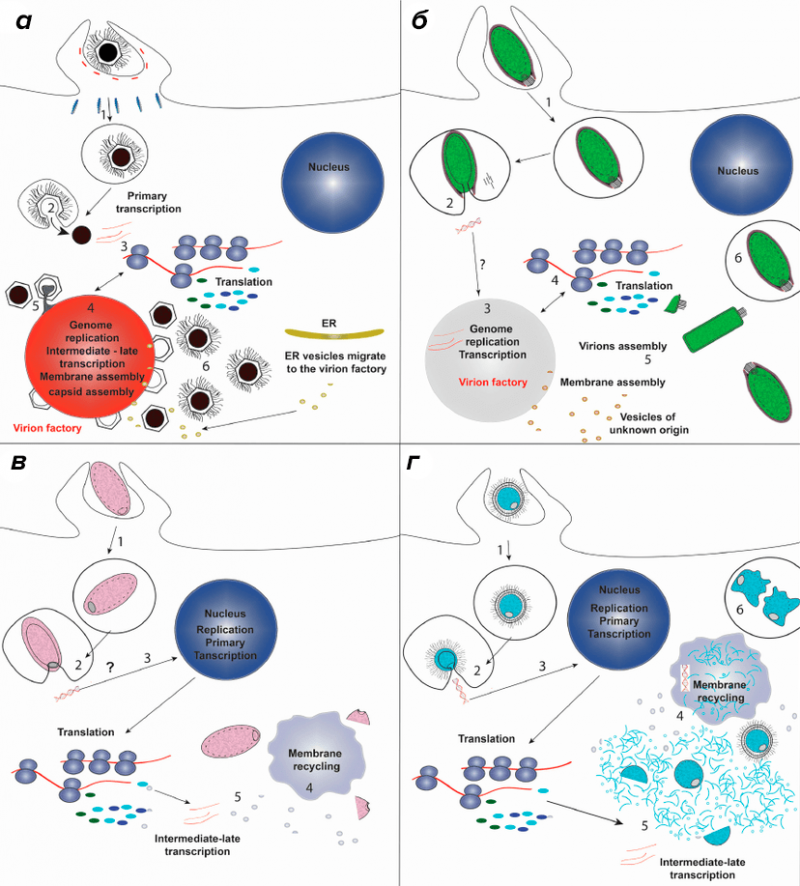
Как правило, вирусы образуют связь с поверхностью клетки, в которой они паразитируют. Далее вирус проникает внутрь и начинает поиск конкретной структуры, которую он способен поразить. Например, возбудители гепатита функционируют и обитают лишь в клеточных единицах печени, а паротит старается проникнуть в околоушные железы.
ДНК (РНК), принадлежащая вирусу, попав внутрь клетки-носителя, начинает взаимодействовать с аппаратом генетической наследственности так, что сама клетка начинает неконтролируемый процесс синтеза специфического ряда белков, зашифрованных в нуклеиновой кислоте самого возбудителя болезни. Далее происходит репликация, выполняемая непосредственно уже самой клеткой, и таким образом начинается процесс сборки новой вирусной частички.
Чем занимается вирион?
Ничем. Именно из-за того, что вирионы не затрачивают энергии, не потребляют ее, ничем не питаются и никак не движутся, им отказывают в праве называться живыми в полном смысле этого слова. Жизни в них не больше, чем в градинах или каплях дождя, — сплошное повиновение законам химии и физики без малейшей инициативы. При этом и ученый, смотрящий на кипучую деятельность вирусов в электронный микроскоп, и фермер, мрачно наблюдающий за веселым танцем градин в его любимой кукурузе, с трудом отделываются от ощущения, что все это безобразие еще какое живое и энергичное!
Одни вирусы могут существовать только внутри живых организмов, другие — прекрасно путешествуют по миру в слюне, соке, пыльце, слезах, фекалиях и прочих временных ковчегах, которые эти организмы оставляют после себя. Есть и вирусы, способные почти бесконечно долго существовать посреди пустынь и полярных айсбергов. Огромное количество вирусов обитает в воде, прежде всего морской; в одной чайной ложке морской воды, взятой с поверхности, будет плескаться не менее миллиона вирионов. (Это не повод отныне заходить в море только в скафандре: тамошние вирусы специализируются в основном по бактериям, водорослям и вообще по планктону, а твои клетки им до лампочки.) Как и было сказано, вирус вне клеток хозяина ничего не делает, просто ждет своего часа. Этот час наступает, когда вирус оказывается рядом с подходящей ему клеткой. Обычно он покрыт разнообразными шипами, крючками и наростиками из разных типов белков, которые умеют определять близость правильной клетки и цепляться к ней. Дальше вирусы действуют по-разному: либо они пробираются внутрь клетки, либо прирастают к ней, либо просто впрыскивают свой генетический материал в клетку. Отныне эта клетка будет продуцировать копии вируса по предоставленным схемам, используя для этого свою энергию и свой строительный материал. Продуцировать — и выпускать в мир. Иногда клеткам и организму эта деятельность никак не мешает. Иногда ему даже полезна. А иногда она его убивает.
Вне клеток вирусы размножаться не умеют. Тем не менее вирусы существуют, и вполне успешно: это самая распространенная форма жизни-нежизни на Земле. Человек пока не очень хорошо изучил эту форму, мы умеем более или менее точно определять лишь около 6000 видов вирусов. Но считается, что их гораздо больше совокупного количества видов всех живых существ на Земле: и бактерий, и других животных, и растений. И нет ни одного живого существа, в котором бы эти вирусы не были расквартированы буквально повсюду. Есть даже такие, которые паразитируют на других вирусах, их называют вирусами-сателлитами и вирофагами.
Даже наши собственные геномы состоят в том числе и из всяких выродившихся вирусов, которые некогда туда проникли и теперь копируются из поколения в поколение — без цели и без смысла. По крайней мере, раньше считалось, что без цели, хотя теперь появились свидетельства, что некоторые казавшиеся пассивными вирусы и их ошметки в нашей ДНК оказывают куда большее влияние на нас и наше здоровье — например, способствуют отбору тех или иных генов при зачатии и «включению» их. Но там пока темна вода во облацех и черт ногу сломит, так что не будем углубляться.
Систематика бактериофагов
Большое количество выделенных и изученных бактериофагов определяет необходимость их систематизации. Этим занимается Международный комитет по таксономии вирусов (ICTV). В настоящее время, согласно Международной классификации и номенклатуре вирусов, бактериофаги разделяют в зависимости от типа нуклеиновой кислоты и морфологии.
На данный момент выделяют девятнадцать семейств. Из них только два РНК-содержащих и только пять семейств имеют оболочку. Из семейств ДНК-содержащих вирусов только два семейства имеют одноцепочечные геномы. У девяти ДНК-содержащих семейств геном представлен кольцевой ДНК, а у других девяти — линейной. Девять семейств специфичны только для бактерий, остальные девять только для архей, а (Tectiviridae) инфицирует как бактерий, так и архей.
| Порядок | Семейство | Морфология | Нуклеиновая кислота | Пример |
|---|---|---|---|---|
| Caudovirales | Myoviridae | Без оболочки, сократительный хвост | Линейная дцДНК | Фаг Т4, фаг μ, PBSX, P1Puna-like, P2, I3, Bcep 1, Bcep 43, Bcep 78 |
| Siphoviridae | Без оболочки, несократительный хвост (длинный) | Линейная дцДНК | Фаг λ, фаг T5, phi, C2, L5, HK97, N15 | |
| Podoviridae | Без оболочки, несократительный хвост (короткий) | Линейная дцДНК | Фаг T7, фаг T3, P22, P37 | |
| Ligamenvirales | Lipothrixviridae | В оболочке, палочкообразные | Линейная дцДНК | Вирус »Acidianus filamentous» 1 |
| Rudiviridae | Без оболочки, палочкообразные | Линейная дцДНК | Палочкообразный вирус »Sulfolobus islandicus» 1 | |
| Неизвестен | Ampullaviridae | В оболочке, бутылкообразные | Линейная дцДНК | |
| Bicaudaviridae | Без оболочки, лемонообразные | Кольцевая дцДНК | ||
| Clavaviridae | Без оболочки, палочкообразные | Кольцевая дцДНК | ||
| Corticoviridae | Без оболочки, изометрические | Кольцевая дцДНК | ||
| Cystoviridae | В оболочке, сферические | Сегментированная дцРНК | ||
| Fuselloviridae | Без оболочки, лемонообразные | Кольцевая дцДНК | ||
| Globuloviridae | В оболочке, изометрические | Линейная дцДНК | ||
| Guttaviridae | Без оболочки, яйцевидные | Кольцевая дцДНК | ||
| Inoviridae | Без оболочки, нитевидные | Кольцевая оцДНК | M13 | |
| Leviviridae | Без оболочки, изометрические | Линейная оцРНК | MS2, Qβ | |
| Microviridae | Без оболочки, изометрические | Кольцевая оцДНК | ΦX174 | |
| Plasmaviridae | В оболочке, плеоморфные | Кольцевая дцДНК | ||
| Tectiviridae | Без оболочки, изометрические | Линейная дцДНК |
Фаговый дисплей
В наши дни бактериофаги широко применяются также в качестве простых систем для наработки белков с заданными свойствами. Речь идет о разработанной в 1980-х гг. крайне эффективной молекулярно-селекционной методике — фаговом дисплее. Этот термин был предложен американцем Дж. Смитом, который доказал, что на основе бактериофагов кишечной палочки можно создать жизнеспособный модифицированный вирус, несущий на своей поверхности чужеродный белок. Для этого в фаговый геном внедряется соответствующий ген, который сливается с геном, кодирующим один из поверхностных вирусных белков. Такие модифицированные бактериофаги можно выделить из смеси с фагами дикого типа благодаря способности «чужого» белка связываться со специфичными антителами (Smith, 1985).
Из экспериментов Смита последовало два важных вывода: во-первых, используя технологию рекомбинантных ДНК, можно создавать огромные по разнообразию популяции численностью 106–1014 фаговых частиц, каждая из которых несет на своей поверхности разные варианты белков. Такие популяции назвали комбинаторные фаговые библиотеки. Во-вторых, выделив из популяции конкретный фаг (например, обладающий способностью связываться с определенным белком или органической молекулой), можно этот фаг размножить в бактериальных клетках и получить неограниченное число потомков с заданными свойствами.
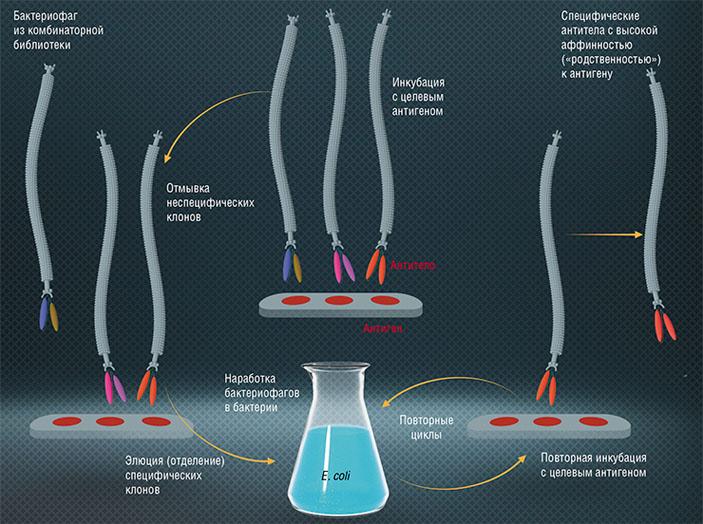
С помощью фагового дисплея сегодня производят белки, которые могут избирательно связываться с терапевтическими мишенями, например, экспонированные на поверхности фага М13, способные узнавать и взаимодействовать с опухолевыми клетками. Роль этих белков в фаговой частице заключается в «упаковке» нуклеиновой кислоты, поэтому они хорошо подходят для создания препаратов генотерапии, только в этом случае они формируют частицу уже с терапевтической нуклеиновой кислотой.
На сегодня можно выделить два основных направления применения фагового дисплея. Технология на основе пептидов используется для исследования рецепторов и картирования сайтов связывания антител, создания иммуногенов и нановакцин, а также картирования сайтов связывания субстратов у белков-ферментов. Технология на основе белков и белковых доменов — для отбора антител с заданными свойствами, изучения белок-лигандных взаимодействий, скрининга экспрессируемых фрагментов комплементарной ДНК и направленных модификаций белков.
С помощью фагового дисплея можно вносить узнающие группировки во все виды поверхностных вирусных белков, а также в основной белок, формирующий тело бактериофага. Вводя в поверхностные белки пептиды с заданными свойствами, можно получить целый спектр ценных биотехнологических продуктов. Например, если этот пептид будет имитировать белок опасного вируса или бактерии, узнаваемый иммунной системой, то такой модифицированный бактериофаг представляет собой вакцину, которую можно просто, быстро и безопасно наработать.
Если же концевой поверхностный белок бактериофага «адресовать» на раковые клетки, а к другому поверхностному белку присоединить репортерные группы (например, флуоресцирующие или магнитные), то получится средство для обнаружения опухолей. А если к частице присоединить еще и цитотоксический препарат (а современная биоорганическая химия позволяет легко это сделать), то получится лекарство, направленно действующее на раковые клетки.
Одним из важных применений метода фагового дисплея белков является создание фаговых библиотек рекомбинантных антител, где антигенсвязывающие фрагменты иммуноглобулинов расположены на поверхности фаговых частиц fd или М13. Особый интерес представляют библиотеки антител человека, поскольку такие антитела могут быть использованы в терапии без ограничения. В последние годы только на фармацевтическом рынке США продается около полутора десятка терапевтических антител, сконструированных с использованием этого метода.
Борцы с патогенами
Первые попытки использовать бактериофаги для лечения инфекционных заболеваний были предприняты практически сразу после их открытия, однако недостаток знаний и несовершенные биотехнологии того времени не позволили достичь полного успеха. Тем не менее дальнейшая клиническая практика показала принципиальную возможность успешного применения бактериофагов при инфекционных заболеваниях желудочно-кишечного тракта, мочеполовой системы, при острых гнойно-септических состояниях больных, для лечения хирургических инфекций и т. д.
По сравнению с антибиотиками бактериофаги имеют ряд преимуществ: они не вызывают побочных эффектов, к тому же строго специфичны для определенных видов бактерий, поэтому при их использовании не нарушается нормальный микробиом человека. Однако такая высокая избирательность создает и проблемы: чтобы успешно лечить пациента, нужно точно знать инфекционный агент и подбирать бактериофаг индивидуально.
Фаги можно использовать и профилактически. Так, Московский научно-исследовательский институт эпидемиологии и микробиологии им. Г. Н. Габричевского разработал профилактический продукт «ФУДФАГ» на основе коктейля из бактериофагов, снижающий риск заражения острыми кишечными инфекциями. Клинические исследования показали, что недельный прием препарата позволяет избавиться от гемолизирующей кишечной палочки и других патогенных и условно-патогенных бактерий, вызывающих дисбактериоз кишечника.
Бактериофагами лечат инфекционные болезни не только людей, но и домашних и сельскохозяйственных животных: мастит у коров, колибактериоз и эшерихиоз у телят и свиней, сальмонеллез у кур… Особенно удобно применять фаговые препараты в случае аквакультуры — для лечения промышленно выращиваемых рыб и креветок, так как в воде они долго сохраняются. Бактериофаги помогают защитить и растения, хотя применение фаговых технологий в этом случае затруднено из-за воздействия природных факторов, таких как солнечный свет и дождь, губительных для вирусов.
Фаги могут сыграть большую роль в поддержании микробиологической безопасности продуктов питания, так как применение антибиотиков и химических агентов в пищевой отрасли не решает эту проблему, одновременно снижая уровень экологической чистоты продукции. О серьезности самой проблемы говорят статистические данные: например, в США и России ежегодно регистрируется до 40 тыс. заболевших сальмонеллезом, из которых 1% умирает. Распространение этой инфекции в значительной степени связано с выращиванием, переработкой и потреблением различных видов птицы, и попытки применить для борьбы с ней бактериофаги дали многообещающие результаты.
Так, американская компания Intralytix производит фаговые препараты для борьбы с листериозом, сальмонеллезом и бактериальным загрязнением кишечной палочкой. Они разрешены к применению как добавки, предотвращающие размножение бактерий на продуктах питания — их распыляют на продукты из мяса и домашней птицы, а также на овощи и фрукты. Эксперименты показали, что коктейль из бактериофагов может быть успешно применен и при транспортировке и реализации живой прудовой рыбы для снижения бактериального загрязнения не только воды, но и самой рыбы.
Очевидным применением бактериофагов является дезинфекция, то есть уничтожение бактерий в тех местах, где их не должно быть: в больницах, на пищевых производствах и т. п. Для этой цели британская компания Fixed-Phage разработала метод фиксации фаговых препаратов на поверхностях, обеспечивающий сохранение биологической активности фагов до трех лет.
Строение бактериофагов
1 — головка, 2 — хвост, 3 — нуклеиновая кислота, 4 — капсид, 5 — «воротничок», 6 — белковый чехол хвоста, 7 — фибрилла хвоста, 8 — шипы, 9 — базальная пластинка
Бактериофаги различаются по химической структуре, типу нуклеиновой кислоты, морфологии и характеру взаимодействия с бактериями. По размеру бактериальные вирусы в сотни и тысячи раз меньше микробных клеток.
Типичная фаговая частица (вирион) состоит из головки и хвоста. Длина хвоста обычно в 2—4 раза больше диаметра головки. В головке содержится генетический материал — одноцепочечная или двуцепочечная РНК или ДНК с ферментом транскриптазой в неактивном состоянии, окружённая белковой или липопротеиновой оболочкой — капсидом, сохраняющим геном вне клетки.
Нуклеиновая кислота и капсид вместе составляют нуклеокапсид. Бактериофаги могут иметь икосаэдральный капсид, собранный из множества копий одного или двух специфичных белков. Обычно углы состоят из пентамеров белка, а опора каждой стороны из гексамеров того же или сходного белка. Более того, фаги по форме могут быть сферические, лимоновидные или плеоморфные.
Хвост, или отросток, представляет собой белковую трубку — продолжение белковой оболочки головки, в основании хвоста имеется АТФаза, которая регенерирует энергию для инъекции генетического материала. Существуют также бактериофаги с коротким отростком, не имеющие отростка и нитевидные.
Головка округлой, гексагональной или палочковидной формы диаметром 45—140 нм. Отросток толщиной 10—40 и длиной 100—200 нм. Одни из бактериофагов округлы, другие нитевидны, размером 8×800 нм. Длина нити нуклеиновой кислоты во много раз превышает размер головки, в которой находится в скрученном состоянии, и достигает 60—70 мкм. Отросток имеет вид полой трубки, окружённой чехлом, содержащим сократительные белки, подобные мышечным. У ряда вирусов чехол способен сокращаться, обнажая часть стержня. На конце отростка у многих бактериофагов имеется базальная пластинка, от которой отходят тонкие длинные нити, способствующие прикреплению фага к бактерии. Общее количество белка в частице фага — 50-60%, нуклеиновых кислот — 40-50%.
Фаги, как и все вирусы, являются абсолютными внутриклеточными паразитами. Хотя они содержат всю информацию для запуска собственной репродукции в соответствующем хозяине, у них нет механизмов для выработки энергии и рибосом для синтеза белка. Размер известных фаговых геномов варьирует от нескольких тысяч до 498 тысяч пар оснований (геном фага G, поражающего бацилл).
Разновидности бактериофага
Существует несколько разновидностей бактериофагов, каждый из которых воздействует на определенных возбудителей:
- Стрептококковый бактериофаг грудничкам и детям более старшего возраста назначают для лечения инфекций, вызванных анаэробными бактериями Streptococcaceae. Попадая в организм, они размножаются в дыхательных путях и в пищеварительном тракте. Бактериофаги данного вида назначаются при отите, гайморите, ангине, ларингите, фарингите, бронхите, дисбактериозе, холецистите и некоторых других заболеваниях.
- Колипротейный бактериофаг воздействует на кишечную палочку Этот вид бактерий распространяется в нижних отделах кишечника. Также препарат эффективен в отношении протей (Pr.mirabilis и Pr.vulgaris) – бактерий, относимых к условно-патогенной микрофлоре кишечника, то есть способной при определенных условиях стать болезнетворной. Бактериофаг данного вида назначается при энтероколитах, кольпитах колипротейного происхождения.
- Клебсиеллезный бактериофаг для грудничков и детей постарше назначается при лечении и профилактике инфекций, вызванных бактериальными возбудителями семейств Klebsiella rhinoscleromatis, Klebsiella ozaenae и Klebsiella pneumoniae. Показан при онземе, склероме, заболеваниях желудочно-кишечного тракта, хирургических и урогенитальных инфекций, гнойно-воспалительных процессах в дыхательных путях и полости рта.
- Бактериофаг стафилококковый грудничкам и более старшим детям врачи назначают при заболеваниях ЛОР-органов, пищеварительных и дыхательных путей, урогенитальных и хирургических инфекциях, гнойно-воспалительных процессах.
- Синегнойный бактериофаг активен в отношении бактерий семейства Pseudomonas aeruginosa (синегнойная палочка). Назначается для лечения инфекций различной локализации: в ЛОР-органах, дыхательных путях, пищеварительном тракте, ранах и т. д.
- Сальмонеллезный бактериофаг показан при сальмонелезе.
- Дизентерийный бактериофаг детям назначается при заражении дизентерийной палочкой (Shigella dysenteriae). Она попадает в организм с едой, через органы пищеварения. Показанием для приема данного препарата является бактериальная дизентерия (шигеллез).
- Брюшнотифозный бактериофаг активен в отношении сальмонелл брюшного тифа, или Salmonella typhi. Назначается для лечения и профилактики кишечной инфекции, вызванной данным возбудителем.
Существуют препараты, состоящие из нескольких стерильных фильтратов фаголизатов, они называются поливалентными бактериофагами и широко применяются в педиатрической практике. Поливалентный бактериофаг для детей чаще всего представляет собой Интестифаг или Пиобактерифаг. Первый лечит все инфекции желудочно-кишечного тракта, второй – гнойные воспалительные инфекции.
Некоторые бактерии перекрывают рецепторы связывания фага, например, белка А, или если инфекции и проникновение происходят, бактерии активируют системы модификации рестрикции, а эндонуклеазы расщепляют чужеродную нуклеиновую кислоту. Это основные проблемы фаговой терапии. Решение представляет собой выделение фаговых мутантов, которые способны преодолевать механизмы защиты хозяина и лизировать первоначально нечувствительные штаммы.
Фаготерапия — использование фагов для лечения бактериальных инфекций. Бактериофаги, способные лизировать патогенные бактерии, оказались на переднем крае открытия бактериальных штаммов, устойчивых к резервным антибиотикам. Одно из первых исследований фаготерапии было проведено с годами в странах бывшего Советского Союза; в Грузии до 31 000 детей, страдающих диареей, были включены в исследования.
Две стороны медали
Достоинства
Бактерии теряют чувствительность к действию антибиотиков. Фармацевтическая промышленность неустанно синтезирует другие. Однако известно, что возможности синтеза антибиотиков ограничены. К действию бактериофагов антибиотики приспосабливаются очень тяжело, а, как утверждают специалисты, к комплексу из нескольких бактериофагов микробы не могут выработать резистентность и вовсе. Кроме того, бактериофаги практически не имеют побочного действия, реже вызывают аллергические явления, могут сочетаться с любыми препаратами. Бактериофаги в настоящий момент хорошо зарекомендовали себя при лечении урологических заболеваний, гнойных процессов в хирургии, а также при лечении инфекционных заболеваний кишечника у новорожденных детей.
Недостатки
- К сожалению, недостатков у медицинских бактериофагов тоже немало. Самая главная проблема проистекает из достоинства – высокой специфичности фагов. Каждый бактериофаг инфицирует строго определенный тип бактерий, даже не таксономический вид, а ряд более узких разновидностей, штаммов. Условно говоря, как если бы сторожевая собака начинала лаять только на одетых в черные плащи громил двухметрового роста, а на лезущего в дом подростка в шортах никак не реагировала. Поэтому для нынешних фаговых препаратов нередки случаи неэффективного применения. Препарат, сделанный против определенного набора штаммов и прекрасно лечащий стрептококковую ангину в Смоленске, может оказаться бессильным против по всем признакам такой же ангины в Кемерове. Болезнь та же, вызывается тем же микробом, а штаммы стрептококка в разных регионах оказываются различными.
Для максимально эффективного применения бактериофага необходима точная диагностика патогенного микроба, вплоть до штамма. Самый распространенный сейчас метод диагностики – культуральный посев – занимает много времени и требуемой точности не дает. Быстрые методы – типирование с помощью полимеразной цепной реакции или масс-спектрометрии – внедряются медленно из-за дороговизны аппаратуры и более высоких требований к квалификации лаборантов. В идеале подбор фагов-компонентов лекарственного препарата можно было бы делать против инфекции каждого конкретного пациента, но это дорого и на практике неприемлемо.
- Другой важный недостаток фагов – их биологическая природа. Кроме того, что бактериофаги для поддержания инфекционности требуют особых условий хранения и транспортировки, такой метод лечения открывает простор для множества спекуляций на тему «посторонней ДНК в человеке». И хотя известно, что бактериофаг в принципе не может заразить человеческую клетку и внедрить в нее свою ДНК, поменять общественное мнение непросто.
- Из биологической природы и довольно большого, по сравнению с низкомолекулярными лекарствами (теми же антибиотиками), размера вытекает третье ограничение – проблема доставки бактериофага в организм. Если микробная инфекция развивается там, куда бактериофаг можно приложить напрямую в виде капель, спрея или клизмы, – на коже, открытых ранах, ожогах, слизистых оболочках носоглотки, ушей, глаз, толстого кишечника – то проблем не возникает.
- Но если заражение происходит во внутренних органах, ситуация сложнее. Случаи успешного излечения инфекций почек или селезенки при обычном пероральном приеме препарата бактериофага известны. Но сам механизм проникновения относительно крупных (100 нм) фаговых частиц из желудка в кровоток и во внутренние органы изучен плохо и сильно разнится от пациента к пациенту. Бактериофаги бессильны и против тех микробов, которые развиваются внутри клеток, например возбудителей туберкулеза и проказы. Через стенку человеческой клетки бактериофаг пробраться не может.
Нужно отметить, что противопоставлять применение бактериофагов и антибиотиков в медицинских целях не следует. При совместном их действии наблюдается взаимное усиление противобактериального эффекта. Это позволяет, например, снизить дозы антибиотиков до значений, не вызывающих выраженных побочных эффектов. Соответственно, и механизм выработки у бактерий устойчивости к обоим компонентам комбинированного лекарства почти невозможен.
Расширение арсенала противомикробных препаратов дает больше степеней свободы в выборе методики лечения. Таким образом, научно обоснованное развитие концепции применения бактериофагов в противомикробной терапии – перспективное направление. Бактериофаги служат не столько альтернативой, сколько дополнением и усилением в борьбе с инфекциями.