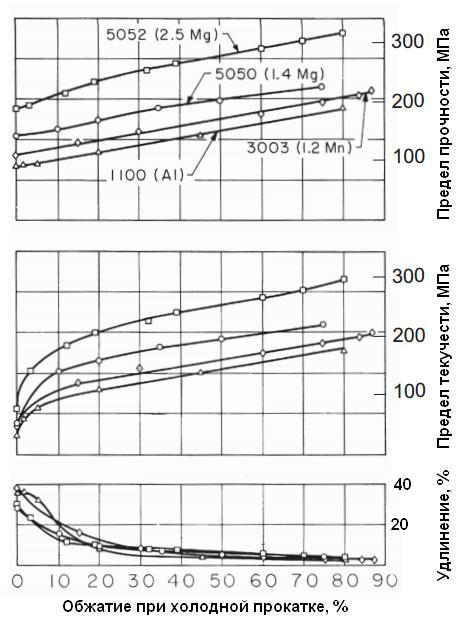
Изотопы углерода
Содержание:
Литература
- Герасимов И. П. Радиоуглеродные исследования Радиометрической лаборатории Института географии АН СССР: Сообщ. 1-5: // Бюллетень Комиссии по изучению четвертичного периода. Сообщ. 1: 1975. № 44. С. 154—159; Сообщ. 2: 1976. № 46. С. 185—189; Сообщ. 3: 1979. № 49. С. 179—187; Сообщ. 4: 1980. № 50. С. 206—213; Сообщ. 5: 1983. № 52. С. 205—211.
- Вагнер Г. А. Научные методы датирования в геологии, археологии и истории: Учебник. — М.: Техносфера, 2006. — 534 с. — ISBN 5-94836-037-7.
- Короновский Н. В. Общая геология: Учебник. — 2-е изд. — М.: Издательство «КДУ», 2010. — С. 122—124. — 526 с. — ISBN 978-5-98227-682-7.
Образование
Углерод-14 образуется в верхних слоях тропосферы и стратосферы в результате поглощения атомами азота-14 тепловых нейтронов, которые в свою очередь являются результатом взаимодействия космических лучей и вещества атмосферы:
- 1n+ 714N→ 614C+ 11H.{\displaystyle \mathrm {~_{0}^{1}n} +\mathrm {~_{7}^{14}N} \rightarrow \mathrm {~_{6}^{14}C} +\mathrm {~_{1}^{1}H} .}
Сечение процесса 14N(n, p)14C довольно высоко (1,83 барн). Оно в 25 раз выше, чем сечение конкурирующего процесса — радиативного захвата теплового нейтрона 14N(n, γ)15N. Существуют и другие реакции, создающие в атмосфере космогенный углерод-14, в частности 13C(n,γ)14C и 17O(n,α)14C. Однако их скорость значительно ниже ввиду меньшей распространённости исходных нуклидов и меньших сечений реакции.
С наибольшей скоростью углерод-14 образуется на высоте от 9 до 15 км на высоких геомагнитных широтах, однако затем он равномерно распределяется по всей атмосфере. В секунду над каждым квадратным метром земной поверхности в среднем образуется от 16 400 до 18 800 атомов углерода-14, хотя скорость образования может колебаться в зависимости от солнечной активности и других факторов. Обнаружены резкие и короткие увеличения скорости образования 14C (события Мияке), предположительно связанные с очень мощной солнечной вспышкой или близким гамма-всплеском, например событие в 774 году н. э., когда в атмосфере одномоментно возникло в три с лишним раза больше радиоуглерода, чем в среднем образуется за год.
Ещё один природный канал образования углерода-14 — происходящий с очень малой вероятностью кластерный распад некоторых тяжёлых ядер, входящих в радиоактивные ряды. В настоящее время обнаружен распад с эмиссией углерода-14 ядер 224Ra (ряд тория), 223Ra (ряд урана-актиния), 226Ra (ряд урана-радия); предсказан, но экспериментально не обнаружен аналогичный процесс для других природных тяжёлых ядер (кластерная эмиссия углерода-14 обнаружена также для отсутствующих в природе нуклидов 221Fr, <sup>221</sup>Ra, <sup>222</sup>Ra и 225Ac). Скорость образования радиогенного углерода-14 по этому каналу пренебрежимо мала по сравнению со скоростью образования космогенного углерода-14.
При испытаниях ядерного и особенно термоядерного оружия в атмосфере в 1940—1960-х годах углерод-14 интенсивно образовывался в результате облучения атмосферного азота тепловыми нейтронами от ядерных и термоядерных взрывов. В результате содержание углерода-14 в атмосфере сильно возросло (так называемый «бомбовый пик», см. рис.), однако впоследствии стало постепенно возвращаться к прежним значениям ввиду ухода в океан и прочие резервуары. Другой техногенный процесс, повлиявший на среднее отношение / в атмосфере, действует в направлении уменьшения этой величины: с началом индустриализации (XVIII век) значительно увеличилось сжигание угля, нефти и природного газа, то есть выброс в атмосферу древнего ископаемого углерода, не содержащего 14C (так называемый ).
Ядерные реакторы, использующие воду в активной зоне, также являются источником техногенного загрязнения углеродом-14.
Общее количество углерода-14 на Земле оценивается в 8500 петабеккерелей (около 50 тонн), в том числе в атмосфере 140 ПБк (840 кг). Количество углерода-14, попавшего в атмосферу и другие среды в результате ядерных испытаний, оценивается в 220 ПБк (1,3 тонны).
Критика метода
Несмотря на то, что радиоуглеродное датирование уже давно вошло в научную практику и достаточно широко используется, в околонаучных публикациях и в Интернете встречается критика этого метода, ставящая под сомнение правомерность его применения для датирования исторических артефактов (в особенности более позднего периода). Как правило, радиоуглеродный метод критикуется сторонниками «научного креационизма» «Новой хронологии» и других псевдонаучных концепций. Некоторые примеры возражений против радиоуглеродного датирования приведены в разделе . Обычно такая критика радиоуглеродного анализа основывается на самых ранних научных публикациях, отражавших состояние методологии в 1960-х годах, и на непонимании основ метода и особенностей калибровки.
Нахождение в природе
Было оценено, что Земля в целом состоит из 730 ppm углерода, с содержанием 2000 ppm в ядре и 120 ppm в мантии и коре. Масса Земли составляет 5,972⋅1024 kg, что предполагает наличие 4360 миллионов гигатонн углерода.
Свободный углерод находится в природе в виде алмаза и графита. Основная масса углерода в виде природных карбонатов (известняки и доломиты), горючих ископаемых — антрацит (94—97 % С), бурые угли (64—80 % С), каменные угли (76—95 % С), горючие сланцы (56—78 % С), нефть (82—87 % С), горючих природных газов (до 99 % метана), торф (53—56 % С), а также битумы и др. В атмосфере и гидросфере находится в виде диоксида углерода СО2, в воздухе 0,046 % СО2 по массе, в водах рек, морей и океанов в ~60 раз больше. Углерод входит в состав растений и животных (~17,5 %).
В организм человека углерод поступает с пищей (в норме около 300 г в сутки).
Общее содержание углерода в организме человека достигает около 21 % (15 кг на 70 кг массы тела). Углерод составляет 2/3 массы мышц и 1/3 массы костной ткани. Выводится из организма преимущественно с выдыхаемым воздухом (углекислый газ) и мочой (мочевина).
Кругооборот углерода в природе включает биологический цикл, выделение СО2 в атмосферу при сгорании ископаемого топлива, из вулканических газов, горячих минеральных источников, из поверхностных слоёв океанических вод, а также при дыхании, брожении, гниении. Биологический цикл состоит в том, что углерод в виде СО2 поглощается из тропосферы растениями в процессе фотосинтеза. Затем из биосферы он вновь возвращается в геосферу, частично через организмы животных и человека, и в виде СО2 — в атмосферу.
В парообразном состоянии и в виде соединений с азотом и водородом углерод обнаружен в атмосфере Солнца, планет, он найден в каменных и железных метеоритах.
Большинство соединений углерода, и прежде всего углеводороды, обладают ярко выраженным характером ковалентных соединений. Прочность простых, двойных и тройных связей атомов С между собой, способность образовывать устойчивые цепи и циклы из атомов С обусловливают существования огромного числа углеродсодержащих соединений, изучаемых органической химией.
В природе встречается минерал шунгит, в котором содержится как твёрдый углерод (≈25 %), так и значительные количества оксида кремния (≈35 %).
Примечания
- Относительная электроотрицательность атома углерода зависит от состояния его гибридизации: Csp3 = 2,5 (в большинстве таблиц) Csp2 = 2,8 Csp1 = 3,2 (алкины)С. Э. Зурабян, Ю. А. Колесник, А. А. Кост и др./под ред. Н. А. Тюкавкиной. Взаимное влияние атомов в молекуле // Органическая химия: Учебник (Учеб. лит. Для учащихся фарм. училищ). — М.: Медицина, 1989. — Т. 1. — С. 36. — 432 с. — ISBN 5-225-00314-1.
- (англ.) (недоступная ссылка). Дата обращения 6 декабря 2007.
- (англ.) (недоступная ссылка). Дата обращения 6 декабря 2007.
- (англ.). Дата обращения 6 декабря 2007.
- ↑ Savvatimskiy, A (2005). «Measurements of the melting point of graphite and the properties of liquid carbon (a review for 1963–2003)». Carbon. 43 (6): 1115–1142. doi:10.1016/j.carbon.2004.12.027
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1. — 623 с.
- .
- Лейпунский О. И. Об искусственных алмазах (рус.) // Успехи химии. — Российская академия наук, 1939. — Вып. 8. — С. 1519—1534.
- Seal M. The effect of surface orientation on the graphitization of diamond. // Phis. Stat. Sol., 1963, v. 3, p. 658.
- Evans T. Changes produced by High Temperature Treatment of Diamond. // The Properties of Diamond. Academi Press, 1979, p. 403–424.
- Андреев В. Д.. Спонтанная графитизация и термодеструкция алмаза при Т > 2000 K // Физика твердого тела, 1999, т. 41, вып. 4, с. 695—201.
- Togaya M. Melting behaviors of carbon underhigh pressure // High Pressure Research, 1990, v. 4, p. 342. (12 AIRAPT Conf. Proc., 1989, Padeborn).
- Андреев В. Д.. Экспериментальные данные по плавлению алмаза и графита с учетом аномальности высокотемпературной теплоёмкости // Химическая физика, 2002, т. 21, № 9, с. 3—11.
- ↑
- . РИА Новости (20190514T1558+0300Z). Дата обращения 14 мая 2019.
- . ТАСС. Дата обращения 14 мая 2019.
- . indicator.ru. Дата обращения 14 мая 2019.
- V. I. Kasatochkin, A. M. Sladkov, et al., Dokl. Akad. Nauk SSSR, 177, No. 2, 358 (1967).
- Р. А. Лидин. Химические свойства неорганических веществ. — Третье. — 2004. — С. 100. — 162 с.
- Минфин РФ. . minfin.ru (27 февраля 2015). — Статистические данные по добыче природных алмазов с 01.01.2003 по 31.12.2014 по результатам сортировки и первичной оценки. Дата обращения 28 июня 2015.
Фракционирование изотопов углерода в природе
В природе разделение изотопов углерода интенсивно происходит при относительно низких температурах. Растения при фотосинтезе избирательно поглощают лёгкий изотоп углерода. Степень фракционирования зависит от биохимического механизма связывания углерода. Большинство растений интенсивно накапливают 12C, и относительное содержание этого изотопа в их составе на 15—25 ‰ выше, чем в атмосфере. В то же время злаковые растения, наиболее распространённые в степных ландшафтах, слабо обогащены 12C и отклоняются от состава атмосферы лишь на 3—8 ‰
Фракционирование изотопов углерода происходит при растворении CO2 в воде и его испарении, кристаллизации и т. п.
Большое число научных работ посвящено изотопному составу углерода алмазов.
Литература
В Викисловаре есть статья «углерод»
- Бухаркина Т. В. Химия природных энергоносителей и углеродных материалов / Т.В. Бухаркина, Н.Г. Дигуров. — М.: РХТУ им. Д.И. Менделеева, 1999. — 195 с. — ISBN 5-7237-0139-8.
- Ола Д.А. Химия гиперкоординированного углерода = Hupercarbon chemistry / Ола Дж., Пракаш Г.К.С., Уильямс Р.Е. и др. Перевод с англ. В.И. Минкина. — М.: Мир, 1990. — 336 с. — ISBN 5-03-001451-9.
- Сладков А. М., Кудрявцев Ю. П. Алмаз, графит, карбин — аллотропные формы углерода // Природа. 1969. № 5. — С.37—44.
- Kirk — Othmer encyclopedia, 3 ed., vol.4, N.-Y., 1978, p. 556—709.
- В.І. Саранчук, В. В. Ошовський, Г. О. Власов. Хімія і фізика горючих копалин . — Донецьк: Східний видавничий дім, 2003. ?204 с.
Ссылки
Изотопы бораПериодическая таблица по изотопам элементовИзотопы азота
| 1H | 2He | ||||||||||||||||
| 3Li | 4Be | 5B | 6C | 7N | 8O | 9F | 10Ne | ||||||||||
| 11Na | 12Mg | 13Al | 14Si | 15P | 16S | 17Cl | 18Ar | ||||||||||
| 19K | 20Ca | 21Sc | 22Ti | 23V | 24Cr | 25Mn | 26Fe | 27Co | 28Ni | 29Cu | 30Zn | 31Ga | 32Ge | 33As | 34Se | 35Br | 36Kr |
| 37Rb | 38Sr | 39Y | 40Zr | 41Nb | 42Mo | 43Tc | 44Ru | 45Rh | 46Pd | 47Ag | 48Cd | 49In | 50Sn | 51Sb | 52Te | 53I | 54Xe |
| 55Cs | 56Ba | * | 72Hf | 73Ta | 74W | 75Re | 76Os | 77Ir | 78Pt | 79Au | 80Hg | 81Tl | 82Pb | 83Bi | 84Po | 85At | 86Rn |
| 87Fr | 88Ra | ** | 104Rf | 105Db | 106Sg | 107Bh | 108Hs | 109Mt | 110Ds | 111Rg | 112Cn | 113Nh | 114Fl | 115Mc | 116Lv | 117Ts | 118Og |
| * | 57La | 58Ce | 59Pr | 60Nd | 61Pm | 62Sm | 63Eu | 64Gd | 65Tb | 66Dy | 67Ho | 68Er | 69Tm | 70Yb | 71Lu |
| ** | 89Ac | 90Th | 91Pa | 92U | 93Np | 94Pu | 95Am | 96Cm | 97Bk | 98Cf | 99Es | 100Fm | 101Md | 102No | 103Lr |
Изотоп 14C
Основная статья: Углерод-14
Помимо стабильных изотопов углерода в природе встречается радиоактивный изотоп 14C (радиоуглерод). Он образуется при облучении <sup>14</sup>N нейтронами по следующей реакции:
- 714N+1n→614C+11H.{\displaystyle \mathrm {{}_{7}^{14}N} +\mathrm {{}_{0}^{1}n} \rightarrow \mathrm {{}_{6}^{14}C} +\mathrm {{}_{1}^{1}H} .}
Кроме азотной реакции, 14C может образовываться при нейтронном облучении изотопа кислорода 17O по реакции 178O + n → 146C + α, однако в атмосфере содержание 17O крайне мало и этот путь образования 14C учитывается только в ядерных технологиях.
В природе 14C образуется в атмосфере из атмосферного азота-14 под действием космического излучения. С небольшой скоростью углерод-14 образуется и в земной коре.
Равновесное содержание 14C в земной атмосфере и биосфере по отношению к стабильному углероду составляет ~10−12. С начала активного использования ископаемого топлива (угля, нефти, газа) в атмосферу постоянно поступает углекислый газ, не содержащий радиоуглерода (распавшегося за миллионы лет), что приводит к постепенному уменьшению отношения 14C/12C в атмосфере; однако это разбавление атмосферного углерода нерадиоактивным ископаемым углеродом (так называемый ) привело за всё время с начала индустриализации (XVIII век) к уменьшению удельной активности 14C в атмосфере лишь на 1,5…2,5 %, а в океанах удельная активность 14C уменьшилась лишь на 0,2 %. Значительно более существенное и резкое изменение, начавшееся в 1945 году, связано с ядерными и особенно термоядерными взрывами в атмосфере, создающими большой поток нейтронов и превращающими атмосферный азот-14 в углерод-14 по вышеприведённой реакции. Этот эффект достиг максимума в середине 1960-х; общее содержание 14C в тропосфере Северного полушария увеличилось почти вдвое. После запрета ядерных испытаний в атмосфере тропосферное содержание 14C стало быстро уменьшаться (двукратное снижение каждые 12—16 лет) вследствие прихода к равновесию тропосферного резервуара с океаном, который обладает значительно большей ёмкостью, чем атмосфера, и почти не был затронут «бомбовым» радиоуглеродом. К настоящему времени атмосферное содержание 14C практически вернулось к значениям доядерной эры, составлявшим (на 1950 год, в пересчёте на удельную активность 14C), 226 Бк на 1 кг атмосферного углерода.
Образование 14C при ядерных взрывах стало одним из значимых факторов радиационного загрязнения, поскольку углерод участвует в обмене веществ живого организма и может накапливаться в нем.
Радиоуглеродный анализ
Основная статья: Радиоуглеродный анализ
Измерение радиоактивности органических веществ растительного и животного происхождения, обусловленной изотопом 14C, применяется для радиоуглеродного анализа возраста старинных предметов и природных образцов. Темп образования 14C в атмосфере Земли в каждый конкретный год измерен по содержанию данного изотопа в образцах с известными датировками, в различных годичных кольцах деревьев и пр. Поэтому и доля 14C в углеродном балансе тоже известна. Живой организм, поглощая углерод, поддерживает баланс 14C идентичным с окружающим миром. После гибели обновление углерода прекращается, и доля 14C постепенно уменьшается вследствие радиоактивного распада. Определяя количество 14C в образце, ученые могут оценить, как давно жил этот организм.
Калибровка
Калибровочная кривая 1998 года, использовавшаяся при радиоуглеродном датировании (Stuiver et al. 1998)
Уточнённая калибровочная кривая 2013 года IntCal13 для диапазона 0—50000 лет до настоящего времени, северное полушарие (Reimer et al. 2013)
Исходные предположения Либби, на которых строится метод радиоуглеродного датирования, заключаются в том, что соотношение изотопов углерода в атмосфере во времени и пространстве не меняется, а содержание изотопов в живых организмах в точности соответствует текущему состоянию атмосферы. Однако, как было установлено в дальнейшем, эти предположения справедливы лишь приблизительно. Содержание изотопа 14C в атмосфере зависит от многих факторов, таких как:
- интенсивность космических лучей и активности Солнца;
- широта местности;
- состояние атмосферы и магнитосферы;
- вулканическая деятельность (углерод, содержащийся в вулканических выбросах, «древний», практически не содержащий 14C);
- круговорот углекислого газа в природе;
- проведение атмосферных ядерных испытаний, создавших в 1950—1960-х годах существенный выброс (около 0,5 тонны) радиоуглерода в атмосферу (бомбовый эффект);
- сжигание большого количества ископаемых топлив (углерод, содержащийся в нефти, природном газе и угле — «древний», практически не содержащий 14C) — так называемый , возникший с началом промышленной революции в XIX веке.
Два последних фактора делают невозможным проведение точных радиоуглеродных датировок у образцов XX века.
Кроме того, исследования показали, что из-за разницы в атомных массах изотопов углерода химические реакции и процессы в живых организмах идут с немного разными скоростями, что нарушает естественное соотношение изотопов (так называемый эффект изотопного фракционирования). Ещё один важный эффект (резервуарный эффект) — замедленное достижение радиоуглеродного равновесия в Мировом океане из-за его медленного обмена углеродом с атмосферным резервуаром — приводит, если не учитывать поправок, к кажущемуся увеличению возраста остатков морских организмов, а также тех сухопутных организмов, чья диета в основном состояла из морской пищи. Понимание процессов, связанных с углеродным обменом в природе и влиянием этих процессов на соотношение изотопов в биологических объектах, было достигнуто не сразу. Таким образом, использование радиоуглеродного метода без учёта этих эффектов и вносимых ими поправок способно породить значительные ошибки (порядка тысячелетия), что часто происходило на ранних этапах развития метода, до 1970-х годов.
В настоящее время для правильного применения метода произведена тщательная калибровка, учитывающая изменение соотношения изотопов для различных эпох и географических регионов, а также специфику накопления радиоактивных изотопов в живых существах и растениях. Для калибровки метода используется определение соотношения изотопов для предметов, абсолютная датировка которых заведомо известна. Одним из источников калибровочных данных является дендрохронология. Также проведены сопоставления определения возраста образцов радиоуглеродным методом с результатами других изотопных методов датирования. Сейчас в качестве стандартной калибровочной кривой используется IntCal, первая версия которой опубликована в 1998 году (см. рис.). Следующие уточнённые версии калибровочной кривой, используемой для пересчёта измеренного радиоуглеродного возраста образца в абсолютный возраст, опубликованы в 2004, 2009 и 2013 году. Калибровочная кривая IntCal13 построена отдельно для северного и южного (SHCal13) полушарий, она охватывает последние 50 000 лет и получена на основании тысяч измерений точно датируемых древесных колец деревьев (последние 12 000 лет), годовых приростов кораллов и отложений фораминифер. Сравнение отложений на дне японского озера Суйгецу за период с 12 000 до 40 тысяч лет назад с информацией, полученной дендрохронологами при анализе древесных колец, привело к внесению поправок, сдвинувших данные в прошлое на 300—400 лет. Калибровка для морских объектов выполняется по отдельной кривой Marine13, поскольку скорость обмена углерода в морском резервуаре медленнее атмосферного.
Можно констатировать, что в своём современном виде на историческом интервале (от десятков лет до 60—70 тысяч лет в прошлое) радиоуглеродный метод можно считать достаточно надёжным и качественно откалиброванным независимым методом датирования предметов биологического происхождения.
Примечания
- Относительная электроотрицательность атома углерода зависит от состояния его гибридизации: Csp3 = 2,5 (в большинстве таблиц) Csp2 = 2,8 Csp1 = 3,2 (алкины)С. Э. Зурабян, Ю. А. Колесник, А. А. Кост и др./под ред. Н. А. Тюкавкиной. Взаимное влияние атомов в молекуле // Органическая химия: Учебник (Учеб. лит. Для учащихся фарм. училищ). — М.: Медицина, 1989. — С. 36. — 432 с. — ISBN 5-225-00314-1.
- Химическая энциклопедия / Редкол.: Кнунянц И.Л. и др.. — М.: Советская энциклопедия, 1988. — Т. 1. — 623 с.
- Лейпунский О. И. Об искусственных алмазах // Успехи химии. — 1939. — Вып. 8. — С. 1519—1534.
- Seal M. The effect of surface orientation on the graphitization of diamond. // Phis. Stat. Sol., 1963, v. 3, p. 658.
- Evans T. Changes produced by High Temperature Treatment of Diamond. // The Properties of Diamond. Academi Press, 1979, p. 403–424.
- Андреев В. Д.. Спонтанная графитизация и термодеструкция алмаза при Т > 2000 K // Физика твердого тела, 1999, т. 41, вып. 4, с. 695—201.
- Togaya M. Melting behaviors of carbon underhigh pressure // High Pressure Research, 1990, v. 4, p. 342. (12 AIRAPT Conf. Proc., 1989, Padeborn).
- Андреев В. Д.. Экспериментальные данные по плавлению алмаза и графита с учетом аномальности высокотемпературной теплоёмкости // Химическая физика, 2002, т. 21, № 9, с. 3—11.
- V. I. Kasatochkin, A. M. Sladkov, et al., Dokl. Akad. Nauk SSSR, 177, No. 2, 358 (1967).
Физические основания
Основная статья: Углерод-14
1: Образование радиоуглерода 14C. 2: Распад 14C. 3: Условие равновесия для живых организмов и неравновесие для умерших организмов, в которых радиоуглерод распадается без пополнения извне
Углерод, являющийся одной из основных составляющих биологических организмов, присутствует в земной атмосфере в виде стабильных изотопов 12C (98,89 %) и 13C (1,11 %) и радиоактивного 14C, который присутствует в следовых количествах (около 10−10%). Изотоп 14C постоянно образуется в основном в верхних слоях атмосферы на высоте 12—15 км при столкновении вторичных нейтронов от космических лучей с ядрами атмосферного азота:
- n+714N→614C+p.{\displaystyle n+\mathrm {^{14}_{7}N} \rightarrow \mathrm {^{14}_{6}C} +p.}
В среднем в год в атмосфере Земли образуется около 7,5 кг радиоуглерода при общем его количестве ~75 тонн.
Образование радиоуглерода вследствие естественной радиоактивности на поверхности Земли пренебрежимо мало.
Радиоизотоп углерода 14C подвержен β−-распаду с периодом полураспада T1/2 = 5730 ± 40 лет, постоянная распада λ = 1,209·10−4 год−1:
- 614C→714N+e−+ν¯e.{\displaystyle \mathrm {^{14}_{6}C} \rightarrow \mathrm {^{14}_{7}N} +e^{-}+{\bar {\nu }}_{e}.}
Соотношение радиоактивного и стабильных изотопов углерода в атмосфере и в биосфере примерно одинаково из-за активного перемешивания атмосферы, поскольку все живые организмы постоянно участвуют в углеродном обмене, получая углерод из окружающей среды, а изотопы, в силу их химической неразличимости, участвуют в биохимических процессах практически одинаковым образом.
Удельная активность углерода в живых организмах, обменивающихся углеродом с атмосферным резервуаром, соответствует атмосферному содержанию радиоуглерода и составляет 13,56 ± 0,07 распада в минуту на грамм углерода. С гибелью организма углеродный обмен прекращается. После этого стабильные изотопы сохраняются, а радиоактивный (14C) постепенно распадается, в результате его содержание в останках постепенно уменьшается. Зная исходное соотношение содержания изотопов в организме и определив их текущее соотношение в биологическом материале масс-спектрометрическим методом или измерив активность методами дозиметрии, можно установить время, прошедшее с момента гибели организма.