Особенности гальванических элементов
Содержание:
Литература
- Дуга электрическая — статья из Большой советской энциклопедии.
- Искровой разряд — статья из Большой советской энциклопедии.
- Райзер Ю. П. Физика газового разряда. — 2-е изд. — М.: Наука, 1992. — 536 с. — ISBN 5-02014615-3.
- Родштейн Л. А. Электрические аппараты, Л 1981 г.
- Clerici, Matteo; Hu, Yi; Lassonde, Philippe; Milián, Carles; Couairon, Arnaud; Christodoulides, Demetrios N.; Chen, Zhigang; Razzari, Luca; Vidal, François (2015-06-01). «Laser-assisted guiding of electric discharges around objects». Science Advances 1 (5): e1400111. Bibcode:2015SciA….1E0111C. doi:10.1126/sciadv.1400111. ISSN 2375—2548.
Гальваническая батарея
Гальваническая батарея, электрическая дуга Петрова и вольтов столб А.
Гальванические батареи применяются в тех случаях, когда необходимо более высокое напряжение или большая емкость по сравнению с напряжением и емкостью одного элемента. Для удобства в эксплуатации промышленность выпускает готовые батареи, удовлетворяющие типовым условиям. Так, например, выпускаются батареи высокого напряжения при малой емкости или низкого напряжения и сравнительно большой емкости.
Гальванические батареи большой емкости используются обычно для создания электрических полей в земле в методах электроразведки.
Широко применяются гальванические батареи для питания репортерских магнитофонов.
|
Принципиальная схема омметра на полупроводниковых триодах. |
Источником питания служит гальваническая батарея для карманного фонаря. Перед измерением устанавливают показывающий прибор ( микроамперметр) на нулевую отметку с помощью переменного сопротивления в цепи питания.
Для операции нужна гальваническая батарея по крайней мере 22 5 V. Положительный полюс прикладывают к коже больного. Активный — отрицательный — электрод представляет собой платиновую иглу диаметром 0 18 мм и длиной 1 5 — 2 мм. Наиболее удовлетворительные результаты дает ток 5 гпА, действующий в продолжение 5 секунд.
По типу электролита гальванические батареи делятся на сухие, наливные и с твердым электролитом.
В заключение, сравнивая гальванические батареи и аккумуляторы, следует подчеркнуть, что преимуществом использования батарей является полная независимость от посторонних источников энергии, что особенно важно при работе в полевых условиях. Основной недостаток их заключается в том, что они имеют малый срок службы, а также большое и непостоянное внутреннее сопротивление, возрастающее по мере разряда батареи.
. Источником питания служат две гальванические батареи КБС-Л-05 или шесть элементов — Марс, 316, 373, обеспечивающие начальное напряжение 9 в
При минимальной громкости приемник потребляет ток 8 — 10 ма, при максимальной мощности — до 25 — 30 ма.
Источником питания служат две гальванические батареи КБС-Л-05 или шесть элементов — Марс, 316, 373, обеспечивающие начальное напряжение 9 в. При минимальной громкости приемник потребляет ток 8 — 10 ма, при максимальной мощности — до 25 — 30 ма.
Затем электроды отъединяются от гальванической батареи и соединяются с гальванометром, для того чтобы наблюдать, идет ли через гальванометр обратный ток, вызванный поляризацией электродов. Такой ток, вызванный накоплением разных веществ на двух электродах, служит доказательством того, что исследуемое вещество было разложено электролитически при прохождении первичного тока от батареи.
Диагональ питания состоит из гальванической батареи Би ( 1 5 в) и двух реостатов Rp и Rf, которые регулируют рабочий ток измерительной схемы.
|
Схема соединений для параллельной работы генераторов с параллельным возбуждением. |
Для питания двигателя была использована гальваническая батарея.
Следует также учитывать, что гальванические батареи имеют значительное внутреннее сопротивление, особенно когда разряжены. При работе импульсного стабилизатора ток, текущий от батареи, модулируется из-за падения напряжения на ее внутреннем сопротивлении, что ведет к уменьшению КПД преобразователя. Конденсатор С1, включенный на входе преобразователя, сглаживает колебания питающего напряжения, несколько повышая КПД. На рис. 2 показана зависимость КПД преобразователя от выходной мощности и напряжения источника питания.
Классификация гальванических элементов

Использованные источники питания различных типов и размеров
Гальванические первичные элементы — это устройства для прямого преобразования химической энергии, заключенных в них реагентов (окислителя и восстановителя), в электрическую. Реагенты, входящие в состав источника, расходуются в процессе его работы, и действие прекращается после расхода реагентов. Примером гальванического элемента является элемент Даниэля—Якоби.
Широкое распространение получили марганцево-цинковые элементы, не содержащие жидкого раствора электролита (сухие элементы, батарейки). Так, в солевых элементах Лекланше: цинковый электрод служит катодом, электрод из смеси диоксида марганца с графитом служит анодом, графит служит токоотводом. Электролитом является паста из раствора хлорида аммония с добавкой муки или крахмала в качестве загустителя.
Щелочные марганцево-цинковые элементы, в которых в качестве электролита используется паста на основе гидроксида калия, обладают целым рядом преимуществ (в частности, существенно большей ёмкостью, лучшей работой при низких температурах и при больших токах нагрузки).
Солевые и щелочные элементы широко применяются для питания радиоаппаратуры и различных электронных устройств.

Литий-ионный аккумулятор сотового телефона
Вторичные источники тока (аккумуляторы) — это устройства, в которых электрическая энергия внешнего источника тока превращается в химическую энергию и накапливается, а химическая — снова превращается в электрическую.
Одним из наиболее распространённых аккумуляторов является свинцовый (или кислотный). Электролитом является 25—30 % раствор серной кислоты. Электродами кислотного аккумулятора являются свинцовые решётки, заполненные оксидом свинца, который при взаимодействии с электролитом превращается в сульфат свинца (II) — PbSO4.
Также существуют щёлочные аккумуляторы: наибольшее применение получили никель-кадмиевые и никель-металлгидридные аккумуляторы, в которых электролитом служит гидроксид калия (K-OH).
В различных электронных устройствах (мобильные телефоны, планшеты, ноутбуки), в основном, применяются литий-ионные и литий-полимерные аккумуляторы, характеризующиеся высокой ёмкостью и отсутствием эффекта памяти.
Электрохимические генераторы (топливные элементы) — это элементы, в которых происходит превращение химической энергии в электрическую. Окислитель и восстановитель хранятся вне элемента, в процессе работы непрерывно и раздельно подаются к электродам. В процессе работы топливного элемента, электроды не расходуются. Восстановителем является водород (H2), метанол (CH3OH), метан (CH4); в жидком или газообразном состоянии. Окислителем обычно является кислород — из воздуха или чистый.
В кислородно-водородном топливном элементе со щёлочным электролитом, происходит превращение химической энергии в электрическую.
Энергоустановки применяются на космических кораблях: они обеспечивают энергией космический корабль и космонавтов.
Характеристики гальванических элементов
Гальванические элементы характеризуются электродвижущей силой (ЭДС), ёмкостью; энергией, которую он может отдать во внешнюю цепь; сохраняемостью.
- Электродвижущая сила (ЭДС) гальванического элемента зависит от материала электродов и состава электролита. ЭДС описывается термодинамическими функциями протекающих электрохимических процессов в виде уравнения Нернста.
- Электрическая ёмкость элемента — это количество электричества, которое источник тока отдаёт при разряде. Ёмкость зависит от массы реагентов, запасённых в источнике, и степени их превращения; снижается с понижением температуры или увеличением разрядного тока.
- Энергия гальванического элемента численно равна произведению его ёмкости на напряжение. С увеличением количества вещества реагентов в элементе и до определённого предела, с увеличением температуры, энергия возрастает. Энергию уменьшает увеличение разрядного тока.
- Сохраняемость — это срок хранения элемента, в течение которого его характеристики остаются в заданных пределах. Сохраняемость элемента уменьшается с ростом температуры хранения.
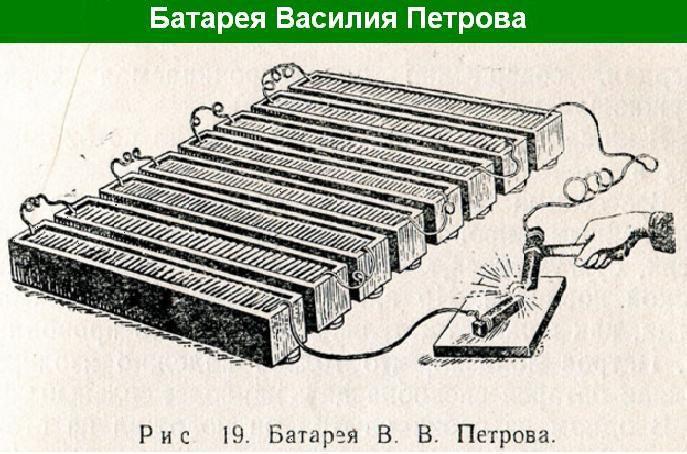
Конструкция батареи Василия Петрова
Профессор Петербургской медицинской академии Василий Владимирович Петров занимался изучением теории электричества. Он глубоко изучил труды Вольта и сделал перевод их на русский язык. Петров изучал различные приборы, построенные по принципу Вольтова столба. Он проводил многочисленные опыты с различными материалами пластин и вариантами электролитов. Он решил создать очень мощный источник электричества. В 1802 году на деньги медицинской академии Петров начал создание самой большой гальванической батареи.
Батарея Василия Петрова имела большие размеры. Основными элементами батареи стали 4200 медных и цинковых дисков размером 35 миллиметров. В качестве электролита использовался нашатырный спирт.

Конструктивно батарея состояла из деревянного ящика, изготовленного из твердой древесины красного дерева. Ящик был покрыт изолирующим слоем из различных смол. Гальванические элементы состояли из металлических дисков и бумажных кружков, пропитанных нашатырным спиртом. Элементы располагались горизонтально в несколько рядов.
Батарея имела надежную жесткую конструкцию и могла использоваться многократно. Батарея создавала очень мощное напряжение, по различным оценкам от 1500 до 1700 Вольт.
Петров фактически был первым, кто провел широкие исследования по теории электролиза как процесса выделения на электродах частей электролита под воздействием электрического тока. Ему удалось выяснить, что различные химические вещества и соединения ведут себя различным образом под действием электричества. Он провел электролиз некоторых веществ. Он установил, что для разных веществ требуется разное напряжение для осуществления процесса электролиза. Так для разложения воды требуется низкое напряжение в несколько вольт, а для электролиза масла необходимо около 1000 Вольт.
Василий Петров установил связь между эффективностью электролиза и температурой окружающей среды. При более высокой температуре электролиз шел активнее. А аккумуляторная батарея давала больше тока.
Применение
- Гальванические элементы используются в системе сигнализации, фонарях, часах, калькуляторах, аудиосистемах, игрушках, радио, автооборудовании, пультах дистанционного управления, компьютерах.
- Аккумуляторы используются для запуска двигателей машин; возможно так же и применение в качестве временных источников электроэнергии в местах, удалённых от населенных пунктов.
- Топливные элементы применяются в производстве электрической энергии (на электрических станциях), аварийных источниках энергии, автономном электроснабжении, транспорте, бортовом питании, мобильных устройствах.
Нередко, химические источники тока применяются в составе батарей (батареек).
История светодиода: два ленинградца, два открытия
Свечение Лосева
В начале тридцатых годов XX века, когда «Светлана» успешно наращивает выпуск ламп накаливания и одновременно превращается в крупнейшее производство электровакуумных приборов различного назначения, молодой советский ученый и изобретатель Олег Лосев, изучая закономерности эффекта электролюминесценции кристаллов карбида кремния, предвосхищает будущую историю светодиода, названного им «Световое реле», на которое он получил в 1929 году Патент № 21291 с приоритетом от 1927 года.
Тогда же ученый переезжает в Ленинград, где продолжает в Физико-техническом институте АН СССР исследования своего открытия. Однако, после смерти Олега Владимировича во время блокады в январе 1942 года, работы на долгое время прекращаются.
И за границей, и в Советском союзе делались попытки практического использования «свечения Лосева», однако отсутствие необходимых технологий не позволило найти решения при жизни ученого.
Гетероструктуры академика Алферова
Применение созданных позднее светодиодов было крайне ограниченно. Из-за недостаточной яркости их широко использовали в различных индикаторах, а об использовании светодиодов для освещения не было и речи.
Очередной прорыв, сыгравший впоследствии ключевую роль в создании светодиодных источников света, снова был совершен в Ленинграде.
Исследования Жореса Алферова и других ученых Ленинградского Физико-технического института им. А.Ф Иоффе Академии наук показали, что на многослойных тонких пленках полупроводниковых материалов можно формировать сложные структуры (наногетероструктуры), позволяющие многократно увеличить выход световой энергии.
Именно на основе гетероструктур в дальнейшем стали создавать яркие и сверхъяркие светодиоды, которые стало возможным использовать в светотехнике.
В 2000 году за работы по созданию и исследованию полупроводниковых гетероструктур Жорес Иванович Алферов получил Нобелевскую премию по физике.
Биография[править]
Василий Владимирович Петров родился 8 июля 1761 года в городе Обояни (ныне Курской области) в семье священника. Учился сначала в Харьковском коллегиуме, потом в Петербургской учительской гимназии.
В 1788 году Петров едет на Алтай, куда он был назначен учителем математики и физики. Там, в Колывано-Воскресенском горном училище в Барнауле, он преподаёт физику, математику, русский и латинский языки.
В 1791 году переведен в Санкт-Петербург на должность преподавателя математики и русского стиля в инженерном училище при Измайловском полку.
В 1793 году Василий Петров был приглашен Санкт-Петербургской медицинской коллегией преподавать математику и физику в Санкт-Петербургском медико-хирургическом училище при военно-сухопутном госпитале. В 1795 году, при преобразовании этого училища в Медико-хирургическую академию. Хотя Петров не получил высшего образования и не защитил положенных тогда магистерской и докторской диссертаций, он был настолько известен своей преподавательской работой, что его назначили заведующим кафедрой и он получил звание экстраординарного профессора. В течение нескольких лет Петров создал богатый для того времени физический кабинет (631 прибор) на базе коллекции физических приборов Д. П. Бутурлина, купленной у родственников графа в Москве за 28000 руб. Кроме коллекции Бутурлина, он приобрёл редкие приборы у наследников профессора Тереховского, выписал ряд аппаратов из Лондона, по его заказам механики на петербургских заводах построили много оригинальных приборов. Он оказал значительную помощь в комплектовании лаборатории Виленскому университету.
Работа В. В. Петрова оплачивалась крайне скудно, поэтому кроме основной работы, он преподавал математику и физику в Академии художеств и в кадетском корпусе.
В 1803 году В. В. Петров был избран корреспондентом Академии Наук.
В 1807 году было решено учредить четыре академических звания в Медико-хирургической академии, и одним из этих четырёх академиков, по предложению академика Л. Ю.Крафта, избрали В. В Петрова.
Многочисленные физические, химические и метеорологические исследования Петрова опубликованы в изданиях Петербургской Академии Наук. Под редакцией Петрова в 1807 году издан перевод физики Шрадера («Начальные основания физики для употребления в гимназиях»). Этим учебником пользовались до начала 1830-х годов. По отзывам современников, Петров был прекрасным лектором и одарённым руководителем.
В 1810 году В. В Петров избирается почётным членом Эрлангенского физико-математического общества (Германия).
В течении 41 -го года В. В. Петров проработал на одном месте в Медико-хирургической академии. За время своей работы он написал три книги и учебник по физике, которым пользовались в гимназиях всей России на протяжении четверти века. Свои книги и научные статьи Петров писал на русском языке, чтобы их читало как можно больше людей, хотя в то время научные работы было принято писать на латыни.
В. В Петров никогда не заискивал перед начальством, не пытался своими лекциями «развлекать» великосветскую знать, поэтому и не пользовался у неё популярностью.
В последние годы своей жизни Петров потерял зрение из-за катаракты обоих глаз. Катаракту удалили и учёный снова приступил к работе, но в феврале 1833 года был неожиданно уволен в отставку с пенсией 5000 рублей в год. Его преемником в 1834 году был назначен Э. Х. Ленц.
Умер В. В. Петров 3 августа 1834 года.
Примечания
- ↑ Петров Василий Владимирович // Большая советская энциклопедия:
- Петров, Василий Владимирович // Русский биографический словарь : в 25 томах. — СПб.—М., 1896—1918.
- Поскольку в то время ещё не была принята система единиц измерения подобных электротехнических параметров, только в 1951 году в результате опытов, проведённых в Московском энергетическом институте были получены оценки электротехнических характеристик батареи Петрова: электродвижущая сила — от 1600 до 1700 вольт; ток короткого замыкания — от 0,1 до 0,2 ампер; мощность — от 65 до 100 ватт.
- Шателен М. А. Русские электротехники второй половины XIX века. — М.-Л.: Изд. и тип. Госэнергоиздата в Москве, 1949. — 380 с. — С. 49.
- .
Завод «Светлана»
Айваз остро чувствовал веяния эпохи и оказался прав, сделав ставку на электролампочку. Двадцатые годы прошлого века начались с масштабного проекта по электрификации всей страны и учреждения знаменитой ГОЭЛРО — Государственной комиссии по электрификации России.
В 1920 году ламповое отделение завода «Айваз» становится самостоятельным предприятием — заводом «Светлана». В том же году Высший совет народного хозяйства решает расширить производство ламп, что дает «Светлане» мощный импульс развития и, начав восстановление производства в условиях еще продолжавшейся Гражданской войны с 12 тысяч лампочек в июле, уже в декабре завод удваивает результат.
Спустя три года специалисты завода сумели наладить массовый выпуск ламп, и объем производства вырос в 15 раз. В 1926 году себестоимость лампочек «Светлана» снизилась почти вдвое, что окончательно сделало их товаром массового потребления. В 1932 году в Ленинграде на заводе «Светлана» была изготовлена лампа накаливания, ставшая эталоном для световых измерений в СССР.
Научные труды Петрова[править]
Первые научные работы Петрова посвящены химическим исследованиям. Он задался целью проверить на опытах все выводы кислородной теории горения Лавуазье. Опыты, проведённые им описаны в книге «Собрание физико-химических новых опытов и наблюдений» (1801), подтверждают вывод французского учёного о том, что только при участии кислорода возможно горение. Петров показал, что в безвоздушном пространстве могут гореть только те вещества, в которых содержится кислород.
Наиболее известная книга Петрова — «Известия о гальвани-вольтовских опытах, которые производил профессор физики Василий Петров, посредством огромной наипаче баттереи, состоящей иногда из 4200 медных и цинковых кружков и находящейся при Санкт-Петербургской Медико-хирургической академии» (1803). Петров изготовил самую большую в мире гальваническую медно-цинковую батарею и получал от неё электродвижущую силу порядка 1700 вольт.
Важнейшим открытием Петрова явилось получение им электрической дуги (1802). Он описывал это открытие следующим образом: «Естьли на стеклянную плитку или скамеечку со стеклянными ножками будут положены два или три древесных угля, способные для произведения светоносных явлений посредством Гальвани-Вольтовской жидкости, и естьли потом металлическими изолированными направителями, сообщёнными с обоими полюсами огромной батареи, приближать оные один к другому на расстоянии от одной до трёх линей, то является между ними весьма яркие белаго цвета свет или пламя, от которого оные угли скорее или медлительнее загораются и от которого тёмный покой довольно ясно освещён быть может».
Аналогичное явление описал английский химик Гемфри Дэви только через 8 лет в 1810 году. Ему в дальнейшем и приписали открытие электрической дуги.
Петров подробно исследовал свойства электрической дуги и высказывал мысль о том, что она может быть использована для освещения, для сварки металлов и для получения некоторых азотистых соединений. Все эти предвидения учёного получили широкое применение в современной технике.
В. В Петров произвёл много экспериментов по изучению неизвестных в то время законов постоянного тока. В 1801 году он нашёл зависимость силы тока от поперечного сечения проводника. Немецкий физик Георг Ом, работавший на этими проблемами, опубликовал результаты своих опытов на 26 лет позже, только в 1827 году.
В. В. Петровым было исследовано электролитическое действие тока на различные жидкости. Он изучил электропроводность многих веществ — угля, фарфора, серы, растительных масел, представил описания электролиза окислов металлов (ртути, свинца, олова), алкоголя, воды и впервые покрыл проводник слоем изоляции.
Много опытов Петров произвёл по изучению физиологического действия тока и указал на опасность высоких напряжений для жизни. Им проведено исследование электрического разряда в вакууме и найдена зависимость этого явления от материала, формы и полярности электродов, от расстояния между ними и степени разряжения.
Одна из известных работ Петрова «Новые электрические опыты» (1804) посвящена статическому электричеству. В ней он устанавливает новые факты электростатики: электризацию проводников, неустойчивость электризации и её уничтожение влажностью.
В. В. Петров много занимался вопросами свечения тел и исследовал явления люминесценции и хемилюминесценции. Он чётко разделял эти два важнейших и различных по своей природе явления.
Если бы Петров написал свои работы посвящённые проводимыми им исследованиям, на латинском языке и напечатал бы их в академическом журнале, то его имя стало бы известным всему миру, так как в то время все эти исследования были новыми. Книги же В. В. Петрова, издавались на русском языке и поэтому остались незамеченными…
Как учёный Петров был очень осторожен в своих выводах и все свои заключения обосновывал экспериментально.
В. В. Петров первым внедрил новые методы в области преподавания физики. На лекциях он демонстрировал различные опыты и ввёл впервые в России физический практикум для студентов.
Принцип работы
Литиевая батарея известна как «электронный насос» из-за носителей заряда, перемещающихся между двумя электродами во время зарядки и разрядки. Электрическое (насосное) давление или разность потенциалов между положительной и отрицательной клеммами называется напряжением или электродвижущей силой (ЭДС). Свободная энергия, связанная с переносом электронов вокруг внешней цепи и ионов лития между двумя интеркалирующими электродами, связана с разницей в химическом потенциале лития в двух электродах.
Элементы батареи накапливают энергию химически в своих электроактивных материалах. Эта химическая энергия преобразуется в электрическую энергию по требованию, посредством электрохимической реакции окисления-восстановления.
 Аккумуляторная батарейка
Аккумуляторная батарейка
Клетки построены в разряженном состоянии. При зарядке положительный электрод, катод, материал окисляется, ионы Li + де-интеркалируются из слоистого интеркалирующего литиевого источника, например LiCoO2, проходят через электролит.
Когда элемент разряжается, на отрицательном электроде происходит реакция окисления, ионы Li + де-интеркалируются из анода и мигрируют через электролит, чтобы быть повторно интеркалированными в материал катода. Одновременная реакция электрохимического восстановления протекает на положительном электроде и принимает электроны из внешнего контура, ионы Li + из электролита, чтобы преобразовать исходный материал. Переход от электронного тока к ионному току происходит на границе раздела электрод/электролит.
- Реакция восстановления положительного электрода (катода): Li 1 -xCoO 2 + xLi + + xe- → LiCoO2
- Реакция окисления отрицательного электрода (анода): LiC 6 → xLi + + xC6 + e-
- Общая обратимая, окислительно-восстановительная, клеточная реакция: LiC 6 + CoO 2 C6 + LiCoO 2
 Применение ячеек
Применение ячеек















