Эффект мпембы
Содержание:
- При какой температуре вода замерзает
- [править] Анализ парадокса
- Холодная или горячая вода замерзает быстрее?
- Какая превратится в лед быстрее?
- Что быстрее: кипящая или холодная H2O?
- Какая вода быстрее замерзает – горячая или холодная
- Причины, по которым кипяток замерзает быстрее холодной воды
- Нагретые водородные связи способствуют образованию структуры льда
- Примеси в составе воды как фактор, влияющий на исход
- Сравнительные показатели
- Почему?
- Как учёные акцентировали внимание на том, что кипяток замерзает быстрее холодной воды
При какой температуре вода замерзает
Почему вообще происходит замерзание воды? В её составе содержится определённое количество минеральных либо органических частиц. Это, например, могут быть очень мелкие частицы песка, пыли или глины. При снижении температуры воздуха эти частицы являются центрами, вокруг которых образовываются ледяные кристаллы.
Роль ядер кристаллизации могут также выполнять пузырьки воздуха и трещины в ёмкости, где содержится вода. На скорость процесса превращения воды в лёд во многом влияет количество таких центров – если их много, жидкость замерзает быстрее. При обычных условиях, с нормальным атмосферным давлением, вода переходит в твердое состояние из жидкого при температуре 0 градусов.
[править] Анализ парадокса
Парадоксальность эффекта Мпембы в том, что время, в течение которого тело остывает до температуры окружающей среды, должно быть пропорционально разности температур этого тела и окружающей среды. Этот закон был установлен еще Ньютоном и с тех пор много раз подтверждался на практике. В данном же эффекте вода с температурой 100°С остывает до температуры 0°С быстрее, чем такое же количество воды с температурой 35 °С.
Тем не менее, это еще не предполагает парадокс, поскольку эффекту Мпембы можно найти объяснение и в рамках известной физики. Вот несколько вариантов такого объяснения:
- Горячая вода быстрее испаряется из контейнера, уменьшая тем самым свой объем, а меньший объем воды с той же температурой замерзает быстрее. В герметичных контейнерах холодная вода должна замерзать быстрее.
- Наличие снеговой шубы в морозилке холодильника. Контейнер с горячей водой протаивает под собой снег, улучшая тем самым тепловой контакт со стенкой морозилки. Контейнер с холодной водой не протаивает под собой снег. При отсутствии снеговой шубы контейнер с холодной водой должен замерзать быстрее.
- Холодная вода начинает замерзать сверху, ухудшая тем самым процессы теплоизлучения и конвекции, а значит и убыли тепла, тогда как горячая вода начинает замерзать снизу. При дополнительном механическом перемешивании воды в контейнерах холодная вода должна замерзать быстрее.
- Наличие центров кристаллизации в охлаждаемой воде — растворенных в ней веществ. При малом количестве таких центров превращение воды в лед затруднено и возможно даже ее переохлаждение, когда она остается в жидком состоянии, имея минусовую температуру. При одинаковом составе и концентрации растворов холодная вода должна замерзать быстрее.
В опытах Мпембы и Осборна учитывалось четвертое условие, а остальные, по-видимому, нет.
Все эти (а также другие) условия изучались во многих экспериментах, но однозначного ответа на вопрос — какие из них обеспечивают стопроцентное вопроизведение эффекта Мпембы — так и не было получено. Так, например, в 1995 году немецкий физик Давид Ауэрбах изучал влияние переохлаждения воды на этот эффект. Он обнаружил, что горячая вода, достигая переохлажденного состояния, замерзает при более высокой температуре, чем холодная, а значит быстрее последней. Зато холодная вода достигает переохлажденного состояния быстрее горячей, компенсируя тем самым предыдущее отставание. Кроме того, результаты Ауэрбаха противоречили полученным ранее данным, что горячая вода способна достичь большего переохлаждения из-за меньшего количества центров кристаллизации. (При нагревании воды из нее удаляются растворенные в ней газы, а при ее кипячении выпадают в осадок некоторые растворенные в ней соли). Утверждать пока можно только одно — воспроизводство этого эффекта существенно зависит от условий, в которых проводится эксперимент. Именно потому, что воспроизводится он далеко не всегда.
Холодная или горячая вода замерзает быстрее?
Ученые выяснили, что если проводить постоянное перемешивание теплой и холодной воды, то холодная жидкость будет превращаться в лед гораздо быстрее.
Холодная или горячая вода замерзает быстрее:
- Многие ученые считают, что в теплой воде связи между молекулами растянуты, поэтому молекула водорода также объемнее в пространстве. При резком охлаждении воды, эти связи разрываются, с очень резким снижением температуры.
- Именно этим и обусловлено быстрое замерзание теплой воды. Считается, что в горячей жидкости содержится меньше растворенных газов, чем в холодной. Именно из-за изменения состава горячей жидкости, происходит ее быстрое превращение в лед.
- До сих пор однозначного и окончательного ответа по поводу этого парадокса нет. Проводились исследования в 2012-2017 годах, которые подтверждали парадокс или опровергали его. В 2016 году в журнале scientific reports, есть ссылка на материалы, что холодная вода переходит в твердое состояние медленнее, чем нагретая.

Лед
Проводили своеобразные исследования, согласно которым замораживали по 400 мл воды с разной температурой. Согласно этим исследованиям, горячая жидкость быстрее охлаждалась, нежели холодная. В 2017 году была опубликована гипотеза, согласно которой эффект Мпембы, который касается нагрева охлажденной системы, не соответствует равновесию. Поэтому под этот парадокс не подходят все основные законы физики и термодинамики.
Какая превратится в лед быстрее?
При одинаковых внешних факторах скорость кристаллизации пресной воды будет выше, чем соленой. При резком охлаждении молекулы воды начинают сцепляться друг с другом, и формируется осколок льда.
Скорость образования льда из питьевой воды при -43°С составляет одну миллионную секунды (0,000001 с). В нормальных условиях кристаллизация пресной воды начинается при 0°С.
 Поэтому скорость образования льда в природе, исходя из исследований американских ученых, составляет 2,32 секунды.
Поэтому скорость образования льда в природе, исходя из исследований американских ученых, составляет 2,32 секунды.
Соленая вода не имеет четко установленной температуры замерзания. Этот показатель зависит от концентрации растворенных веществ.
Рассчитать показатели, при которых начинается образование льда можно по формуле:
t3 = -0,0545*S, где S – это уровень насыщения воды минеральными веществами.
Результат всегда будет ниже 0 градусов. Кроме этого, механизм образования льда такого раствора отличается от процессов, проходящих в питьевой воде.
Что быстрее: кипящая или холодная H2O?
 Учеными проведено множество экспериментов и доказано, что первой кристаллизуется кипящая вода.
Учеными проведено множество экспериментов и доказано, что первой кристаллизуется кипящая вода.
Если в морозилку одновременно поставить две емкости одинакового объема и формы с кипятком и простой водой, то первым превратится в лед именно кипяток.
Хотя, если следовать логике, он должен сначала остыть, а уже потом кристаллизоваться. Но это не так.
Стоит отметить, что подобный эффект наблюдался людьми давно. На это указывал в своих записях Аристотель, интересовался явлением Р.Декарт. Однако тщательно изучением данного вопроса в то время мало кто занимался, оно не особо интересовало ученых.
В 1969 году профессором Д.Осборном был проведен эксперимент, который доказал утверждения юноши. С того момента феномен получил имя своего «открывателя», и стал называться эффектом Мпембы.
Какая вода быстрее замерзает – горячая или холодная

Вода – одна из самых удивительных жидкостей на свете, которой присущи необычные свойства. Например, лед – твердое состояние жидкости, имеет удельный вес ниже, чем сама вода, что сделало во многом возможным возникновение и развитие жизни на Земле.
Кроме того, в околонаучном, да и научном мире ведутся дискуссии по поводу, какая вода быстрее замерзает – горячая или холодная.
Тот, кто докажет более быстрое замерзание горячей жидкости в определенных условиях и научно обоснует свое решение, получит от Британского королевского общества химиков награду в 1000 фунтов стерлингов.
История вопроса
О том, что при выполнении ряда условий горячая вода по скорости замерзания опережает холодную, было замечено еще в Средневековье. Объяснению этого феномена затратили немало усилий Френсис Бэкон (Francis Bacon) и Рене Декарт (René Descartes).
Однако, с точки зрения классической теплотехники, этот парадокс объяснить невозможно, и о нем старались стыдливо замалчивать. Толчком к продолжению споров послужила несколько курьезная история, случившаяся с танзанийским школьником Эрасто Мпембе (Erasto Mpemba) в 1963 году.
Однажды во время урока по приготовлению десертов в школе поваров, мальчик, отвлекшись на посторонние дела, не успел охладить смесь для мороженого вовремя и сунул в морозильную камеру раствор сахара в молоке горячим.
На его удивление, продукт охладился несколько быстрее, чем у его соучеников, соблюдающих температурный режим приготовления мороженого.
Пытаясь уяснить сущность явления, мальчик обратился к учителю физики, который, не вдаваясь в подробности, высмеял его кулинарные опыты. Однако Эрасто отличался завидным упорством и продолжил свои эксперименты уже не на молоке, а на воде. Он убедился, что в ряде случаев замерзание горячей воды происходит быстрее, чем холодной.
Поступив в университет в Дар-эс-Саламе (University of Dar es Salaam), Эрасто Мпембе посетил лекцию профессора Дениса Г. Осборна (Dennis G. Osborne). После её окончания студент озадачил ученого проблемой о скорости замерзания воды в зависимости от ее температуры. Д.Г.
Осборн высмеял саму постановку вопроса, заявив с апломбом, что любому двоечнику известно, что холодная вода замерзнет быстрее. Однако природное упорство юноши дало о себе знать. Он заключил с профессором пари, предложив здесь же, в лаборатории, провести экспериментальную проверку.
С тех пор это явление получило название «Парадокса Мпембы».
Однако до настоящего времени нет стройной теоретической гипотезы, объясняющей «Парадокс Мпембы». Не ясно, какие внешние факторы, химический состав воды, наличие в ней растворенных газов и минеральных веществ оказывают влияние на скорость замерзания жидкостей, находящихся при разных температурах.
Парадоксальность «Эффекта Мпембы» в том, что он противоречит одному из законов, открытых еще И. Ньютоном, который гласит, что время остывания воды прямо пропорционально разности температур жидкости и окружающей среды.
И если все остальные жидкости полностью подчиняются этому закону, то вода в ряде случаев является исключением.
Почему горячая вода быстрее замерзает
Существует несколько версий, почему горячая вода замерзает быстрее холодной. Основными из них считаются:
- горячая вода быстрее испаряется, при этом уменьшается ее объем, а меньший объем жидкости остывает быстрее – при охлаждении воды от + 100°С до 0°С объемные потери при атмосферном давлении достигают 15%;
- интенсивность теплообмена между жидкостью и окружающей средой тем выше, чем больше разница температур, поэтому тепловые потери кипятка проходят быстрее;
- при остывании горячей воды на ее поверхности образуется корочка льда, препятствующая полному промерзанию жидкости и ее испарению;
- при высокой температуре воды происходит ее конвекционное перемешивание, сокращающее время замерзания;
- растворенные в воде газы понижают точку замерзания, отбирая энергию на кристаллообразование, – в горячей воде растворенные газы отсутствуют.
Все эти условия неоднократно подвергались экспериментальной проверке. В частности, германский ученый Давид Ауэрбах (David Auerbach) обнаружил, что температура кристаллизации горячей воды несколько выше, чем у холодной, что делает возможным более быстрое замерзание первой.
Однако позднее его опыты были подвергнуты критике и многие ученые убеждены, что «Эффект Мпембы» о том, какая вода быстрее замерзает – горячая или холодная, можно воспроизвести только в определенных условиях, поисками и конкретизацией которых до настоящего времени никто не занимался.
Причины, по которым кипяток замерзает быстрее холодной воды
Парадокс Мпембы был замечен уже давно. Об этом странном явлении упоминали философы, натуралисты, физики, начиная со времён Аристотеля.
Учёные выдвигают несколько версий, почему кипяток замерзает быстрее холодной воды. Хотя точная причина этого феномена пока не известна. Ведь горячая и холодная вода обладают разными свойствами. И какие именно приводят к возникновению «Парадокса Мпембы» – учёным выяснить пока не удалось.
Ещё Ньютон вывел закон, что тело остывает до температуры окружающей среды пропорционально разности температур между ними. Но вода, разогретая до 100°С, превращается в лёд гораздо быстрее, чем с температурой в 35°С.
Объём. Горячая вода в процессе нагревания интенсивно испаряется. Это уменьшает её объём. Это способствует сокращению времени на замерзание.
Конвекция. Чем меньше температура воды, тем быстрее в ней образуется лёд. Он мешает процессу теплообмена – конвекции. На языке физики – замерзание представляет собой процесс теплоотдачи. В горячей воде этому процессу ничего не мешает.
Кристаллизация. Кристаллы льда в холодной воде образуется по направлению сверху-вниз. Это затрудняет процесс замерзания. В горячей воде, кристаллы льда начинают формироваться снизу-вверх. Поверхность не покрывается «плёнкой», которая замедляет процесс замерзания.
Теории про кристаллизацию и конвекцию перекликаются между собой. Хотя имеют разный механизм.
Есть и другие теории, которые выдвигались в разный период времени, но они не столь правдоподобны. В любом случае, «Парадокс Мпембы» до сих пор не разгадан.
Нагретые водородные связи способствуют образованию структуры льда
Еще в 2012 г. британское Королевское химическое общество объявило конкурс гипотез, объясняющих этот феномен, получив более 22 тыс. статей от ученых всего мира, однако ни одна из них не убедила большинство членов экспертной комиссии. Наиболее популярным объяснением остается испарение: горячая вода испаряется быстрее холодной, поэтому объем ее уменьшается немного быстрее, облегчая замерзание.
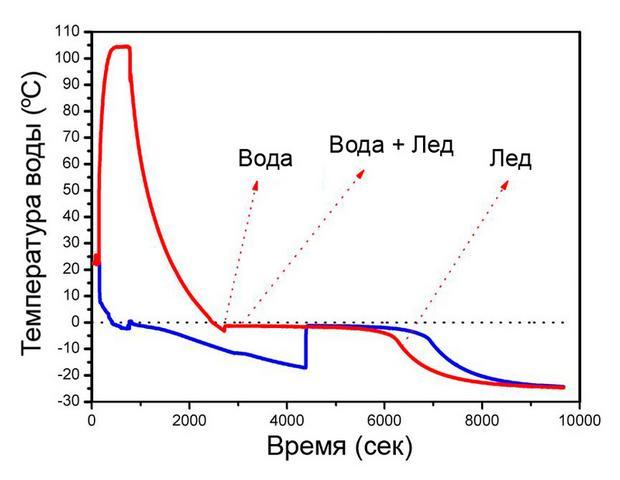
Свойства замерзания горячей (красная линия) и холодной (синяя линия) воды
С другой стороны, и этот вариант нельзя назвать окончательным: эффект Мпембы демонстрировался и в условиях, исключавших испарение. Новое объяснение предложили недавно ученые из Китая и США, статью которых опубликовал Journal of Chemical Theory and Computation.
Авторы смоделировали поведение короткоживущих кластеров молекул воды, объединенных водородными связями, при разных температурах. Водородные связи намного (примерно в 18-20 раз) слабее обычных ковалентных химических взаимодействий, однако сила их зависит от геометрии взаимного расположения молекул, между которыми эти связи образуются.
По мере нагревания водородные связи ослабевают и, как показало моделирование, молекулы воды в кластерах меняют положение, занимая такие позиции, из которых им проще переходить к кристаллической структуре льда. В холодной воде все происходит так же, только энергии на разрыв водородных связей требуется больше – и замерзание, соответственно, должно проходить медленнее.
Примеси в составе воды как фактор, влияющий на исход

Если не жульничать и использовать воду с одинаковым составом, где концентрации определенных веществ являются идентичными, то холодная вода должна замерзнуть быстрее. Но если же происходит ситуация, когда растворённые химические элементы в наличии только в горячей воде, а холодная вода при этом ими не обладает, тогда есть возможность у горячей воды замерзнуть раньше. Объясняется это тем, что растворенные вещества в воде создают центры кристаллизации, и при малом количестве этих центров превращение воды в твердое состоянии затруднено. Возможно даже переохлаждение воды, в том плане, что при минусовой температуре она будет находиться в жидком состоянии.
Но все эти версии, видно, не до конца устраивали ученых и они продолжали работать над этим вопросом. В 2013 году команда исследователей в Сингапуре заявила, что им удалось разгадать вековую загадку.

Сравнительные показатели
Наличие примесей существенно влияет на физические свойства вещества:
- Изменяется плотность,
- температурные режимы,
- поведение при переходах из одного агрегатного состояния в другое.
Температура замерзания
Минерализация питьевой воды составляет 0,1%, поэтому температура замерзания 0 градусов Цельсия. Концентрация минеральных добавок в соленой воде варьируется. Температуру замерзания рассчитывают по формуле t3 = -0,0545*S, то есть изменение происходит на -0,54°С на каждые 10 промилле солености.
Например, при минерализации раствора равной 24,7 промилле (морская вода) показатель равен -1,33°С. В Мертвом море насыщенность минеральными добавками достигает 350 промилле. Вода в нем будет кристаллизоваться при -19° Цельсия.
Почему несоленая замерзнет при 0 градусов, а соленая – меньше 0 градусов?
Соленые и пресные воды отличаются по составу. Это 2 различных раствора. Они отличаются по физическим показателям. Поэтому температуры кристаллизации отличаются.
Факторы и их влияние
На начало процесса образования льда в питьевой воде оказывает влияние 2 фактора – процент растворенных минеральных веществ и давление.
Если количество примесей стремится к нулю, и по физическим показателям питьевая вода приближается к химически чистому веществу, то она может оставаться в жидкой форме при температуре ниже 0 градусов.
Если понизить давление, то процесс кристаллизации замедлится. При изменении показателя на 1 атмосферу температура повышается на 0,01°C.
Факторы, влияющие на температуру образования льда из соленой воды:
- концентрация минеральных веществ;
- внешние условия – погода, наличие ветра, лабораторные условия или естественная среда.
Как происходит кристаллизация в различных растворах?
Процесс кристаллизации жидкости отличается в зависимости от степени ее минерализации:
- Пресная – после образования начального кристалла льда начинается хаотическое изменение ее агрегатного состояния. Могут сформироваться шестиугольный и кубический лед.
Они состоят из гексаэдров с атомами кислорода в вершине, но относительное расположение колец отличается. Кубический лед встречается на высоте несколько тысяч метров
- Соленая – при достижении температуры замерзания образуются ледяные иглы. Часть минеральных веществ остается в образующихся кристаллических структурах. Минерализация такого льда в 4 раза меньше исходного раствора.
Дальнейший процесс зависит от внешних факторов. Соленая вода замерзает, начиная от края емкости, в центре образуется непрозрачный стержень. В нем содержится большая часть минеральных добавок. Эта часть замерзает последней.
Если процесс идет в естественных условиях, то верхняя охлажденная часть будет опускаться вниз. На поверхность поднимаются теплые потоки.
Перемешивание продолжается до тех пор, пока не достигнет точки переохлаждения. После этого соленая вода замерзает иглами на всю глубину.
Почему?
Полностью объяснить и понять явление пока не получилось, но споров среди ученых по данной теме ведется достаточно.
Однако некоторые гипотезы все же имеют место:
- При кипении происходит испарение и уменьшение объема вода, а значит, процесс кристаллизации активизируется, т.е. ускоряется.
- Испаряются растворенные в воде газы, поэтому плотность воды в кипящем состоянии выше, чем у воды комнатной температуры. Известно, что высокий процент плотности способствует скорости охлаждения.
- Замерзание горячей воды начинает идти снизу, и верхний слой поверхности остается свободным. Это позволяет процессам конвекции и излучения тепла не останавливаться и не замедляться. У воды в обычном состоянии сначала промерзает верхняя поверхность, которая тормозит выход тепла.
Есть и другие версии, объясняющие парадоксальное явление. Одно из них было выдвинуто ученым из Вашингтона Д.Катцем. По его мнению, в процессе кипячения вода из «жесткой» превращается в «мягкую».
Часть веществ, такие как магний и бикарбонат кальция, при нагревании оседают и не мешают кристаллизации. Поэтому процесс замерзания кипятка идет в разы быстрее обычной.
Как учёные акцентировали внимание на том, что кипяток замерзает быстрее холодной воды
Однажды, в далёком 1963 году, ученик по имени Эрасто Мпемба – Erasto B. Mpemba, принимал участие в одном кулинарном задании. Оно заключалось в приготовлении мороженого. В тёплом молоке растворяли сахар, остужали до комнатной температуры, и отправляли в морозилку.
Не известно по каким причинам, вероятнее всего, из-за желания побыстрее сделать лакомство, Эрасто отправил в морозильник ещё тёплую смесь. Спустя время, он решил проверить результат своих трудов. Как же удивился мальчика, когда обнаружил – его смесь замёрзла быстрее остальных.
Заинтересовавшись столь необычным, и тем более, не понятным школьнику феноменом, Эрасто задал вопрос о его природе школьному учителю физики. На что тот ответил мальчику в шутливой форме.
Мальчик продолжил эксперименты с водой разного нагрева. Спустя несколько лет ему удалось пообщаться с Денисом Осборном – Denis G. Osborne. Физик из Великобритании приехал в городок Иринга прочитать курс лекций в школе.
Эраст задал Денису Осборну вопрос, который волновал его несколько лет
Физика заинтересовал феномен, на который когда-то обратил внимание мальчик















