Самый громкий бах: какая взрывчатка мощнее всех
Содержание:
- Свойства
- История
- Китайский разрушитель
- Взрывчатка: что это такое?
- Полимерный азот
- Начало в жидком виде
- Гексоген – взрывоопасное лекарство
- Физика горения и взрыва
- Взрывчатка, которая убивает своих
- Астролит – хорош, но дурно пахнет
- Самый мощный взрыв: Оппау, 1921 год
- Использование в качестве взрывчатого вещества
- Физико-химические свойства
Свойства
| Показатель | Стандартные значения |
| Цвет | белый |
| Состав | перекись ацетона, эмпирическая формула C6H12O4 |
| Внешний вид | мелкодисперсный порошок, после длительного хранения — кристаллы правильной формы |
| Запах | резкий характерный |
| Вкус | без вкуса |
| Содержание основного вещества | 96% |
| Растворимость | хорошо в эфире, бензоле, ацетоне, уксусной кислоте. Нерастворим в воде |
| Плотность вещества | 1,3 г/см³ |
| Другие | не гигроскопична; при обычных условиях хранения не разлагается; обладает повышенной летучестью, при комнатной температуре испаряется в течение 2 часов; при нагревании с раствором серной кислоты распадается до ацетона и перекиси водорода; устойчива в кислотных и щелочных растворах; не корродирует металлы (исключение — свинец); проявляет окислительные свойства; плавится при температуре 97ºC. Взрывоопасна! |
История
Первые эксперименты по получению пероксидов ацетона были проведены Вольфенштейном в 1895 году, когда он изучал действие пероксида водорода на кониин в ацетоновом растворе, полагая, что ацетон и пероксид водорода не взаимодействуют. Вольфенштейн обнаружил, что из смеси равных объёмов ацетона и 10%-ного пероксида водорода выпадают кристаллы, которые он охарактеризовал как тримерный пероксид ацетона (триперекись ацетона 2). Также он заметил, что реакция происходит быстрее при добавлении малых количеств фосфорной кислоты.
В 1899 году Адольф Байер и Виктор Виллигер синтезировали также димерный пероксид ацетона (диперекись ацетона 1). В 1933 году Лекок наблюдал процесс деполимеризации трипероксида ацетона при определении его молекулярной массы методом криоскопии, а также при плавлении. В 1947 году изучалось влияние кислот на образование пероксидов ацетона, в частности, было замечено, что серная, соляная, фосфорная и азотная кислоты значительно ускоряют окисление ацетона пероксидом водорода, а в присутствии органических кислот (уксусной, бензойной) образования продукта не происходит.
К настоящему времени получены пероксиды ацетона четырёх структур.
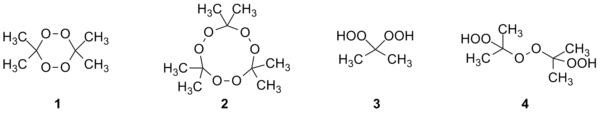
Китайский разрушитель
В 80 годах прошлого века было синтезировано вещество трициклическая мочевина. Считается, что первыми, кто получил эту взрывчатку, были китайцы. Тесты показали огромную разрушительную силу «мочевины» — один её килограмм заменял двадцать два килограмма тротила.
Эксперты соглашаются с такими выводами, поскольку «китайский разрушитель» имеет самую большую плотность из всех известных взрывчатых веществ, и при этом обладает максимальным кислородным коэффициентом. То есть, во время взрыва стопроцентно сжигается весь материал. Кстати, у тротила он равен 0.74.
В реальности трициклическая мочевина не годится для военных действий, прежде всего, из-за плохой гидролитической стойкости. Уже на следующий день при стандартном хранении она превращается в слизь. Впрочем, китайцам удалось получить другую «мочевину» — динитромочевину, которая хоть и хуже по фугасности, чем «разрушитель», но тоже относится к одному из самых мощных взрывчатых веществ. Сегодня ее выпускают американцы на своих трех пилотных установках.
Взрывчатка: что это такое?
Взрывчатые вещества – это большая группа химических соединений или смесей, которые под воздействием внешних факторов способны к быстрой, самоподдерживающейся и неуправляемой реакции с выделением большого количества энергии. Проще говоря, химический взрыв – это процесс преобразования энергии молекулярных связей в тепловую энергию. Обычно его результатом является большое количество раскаленных газов, которые и выполняют механическую работу (дробление, разрушение, перемещение и др.).
Классификация взрывчатых веществ довольно сложна и запутанна. К ВВ относятся вещества, которые распадаются не только в процессе взрыва (детонации), но и медленного или быстрого горения. К последней группе относятся пороха и различные виды пиротехнических смесей.
Детонацией называют стремительное (сверхзвуковое) распространение фронта сжатия с сопутствующей ему экзотермической реакцией во взрывчатом веществе. В этом случае химические превращения идут настолько бурно и выделяется такое количество тепловой энергии и газообразных продуктов, что в веществе образуется ударная волна. Детонация – это процесс максимально быстрого, можно сказать, лавинообразного вовлечения вещества в реакцию химического взрыва.
Дефлаграция, или горение – это тип окислительно-восстановительной химической реакции, во время которой ее фронт перемещается в веществе за счет обычной теплоотдачи. Подобные реакции хорошо всем известны и часто встречаются в повседневной жизни.
Любопытно, что энергия, выделяемая при взрыве, не так уж и велика. Например, при детонации 1 кг тротила ее выделяется в несколько раз меньше, чем при сгорании 1 кг каменного угля. Однако при взрыве это происходит в миллионы раз быстрее, вся энергия выделяется практически мгновенно.

Чтобы запустить процесс химического взрыва необходимо воздействие внешнего фактора, он может быть нескольких видов:
- механический (накол, удар, трение);
- химический (реакция какого-либо вещества с зарядом взрывчатки);
- внешняя детонация (взрыв в непосредственной близости от ВВ);
- тепловой (пламя, нагревание, искра).
Следует отметить, что разные виды ВВ имеют различную чувствительность к внешним воздействиям.
Некоторые из них (например, черный порох) прекрасно реагируют на тепловое воздействие, но при этом практически не откликается на механическое и химическое. А для подрыва тротила нужно только детонационное воздействие. Гремучая ртуть бурно реагирует на любой внешний раздражитель, а есть некоторые ВВ, которые детонируют вообще безо всякого внешнего воздействия. Практическое использование таких «взрывоопасных» ВВ попросту невозможно.
Полимерный азот
Идеальной взрывчаткой могло бы стать соединение, в котором
присутствуют только атомы азота. Создание такого полимерного азота ученые
предсказали еще в начале 90-х. Впервые вещество экспериментально получили в
2004 году в России, однако для его синтеза требуется давление свыше миллиона
атмосфер, что исключает практическое применение такой взрывчатки.
Ученые продолжают поиски самого лучшего взрывчатого вещества
— согласно прогнозам, некоторые виды нитридов, в которых несколько атомов азота
особым образом соединены с атомами хрома, циркония или гафния, могут обладать
чудовищным энергетическим потенциалом, схожим с полимерным азотом.
Начало в жидком виде
История современных взрывчатых веществ начинается в 1846 году, когда итальянский ученый Асканио Собреро впервые получил нитроглицерин — сложный эфир глицерина и азотной кислоты. Собреро достаточно быстро обнаружил взрывчатые свойства бесцветной вязкой жидкости и потому поначалу назвал полученное соединение пироглицерином.
Альфред Нобель — человек, создавший динамит.
Трехмерная модель молекулы нитроглицерина.
По современным представлениям нитроглицерин — весьма посредственная взрывчатка. В жидком состоянии он слишком чувствителен к удару и нагреву, а в твердом (охлажденном до 13°С) — к трению. Фугасность и бризантность нитроглицерина сильно зависят от способа инициирования, а при использовании слабого детонатора мощность взрыва сравнительно невелика. Но тогда это было прорывом — мир еще не знал подобных веществ.
Практическое использование нитроглицерина началось лишь спустя семнадцать лет. В 1863 году шведский инженер Альфред Нобель конструирует пороховой капсюль-воспламенитель, позволяющий использовать нитроглицерин в горном деле. Спустя еще два года, в 1865 году, Нобель создает первый полноценный капсюль-детонатор, содержащий фульминат ртути. При помощи такого детонатора можно инициировать практически любое бризантное взрывчатое вещество и вызвать полноценный взрыв.
В 1867 году появляется первая взрывчатка, пригодная для безопасного хранения и транспортировки, — динамит. Девять лет потребовалось Нобелю на то, чтобы довести технологию производства динамита до совершенства — в 1876 году был запатентован раствор нитроцеллюлозы в нитроглицерине (или «гремучий студень»), который до сегодняшнего дня считается одним из самых мощных взрывчатых веществ бризантного действия. Именно из этого состава готовился знаменитый динамит Нобеля.
Выдающийся химик и инженер Альфред Нобель, фактически изменивший лицо мира и давший реальный толчок развитию современной военной и, косвенно, космической технике скончался в 1896 году, прожив 63 года. Имея слабое здоровье, он так увлекался работой, что часто забывал поесть. На каждом из его заводов строилась лаборатория, чтобы неожиданно приехавший хозяин мог продолжить эксперименты без малейшей задержки. Он был и генеральным директором своих заводов, и главным бухгалтером, и главным инженером и технологом, и секретарем. Жажда познания была основной чертой его характера: «Вещи, над которыми я работаю, действительно чудовищны, но они так интересны, так совершенны технически, что становятся привлекательными вдвойне».
Гексоген – взрывоопасное лекарство
Еще в 1899 году для лечения воспаления в мочевых путях немецкий химик Ганс Геннинг запатентировал лекарство гексоген – аналог известного уротропина. Но вскоре медики потеряли к нему интерес из-за побочной интоксикации. Только через тридцать лет выяснилось, что гексоген оказался мощнейшим взрывчатым веществом, причем, более разрушительным, чем тротил. Килограммовая взрывчатка гексогена произведет такие же разрушения, как и 1.25 килограмм тротила.
Специалисты-пиротехники в основном характеризуют взрывчатые вещества фугасностью и бризантностью. В первом случае говорят об объеме газа, выделенного при взрыве. Мол, чем он больше, тем мощнее фугасность. Бризантность, в свою очередь, зависит уже от скорости образования газов и показывает, как взрывчатка может дробить окружающие материалы.
10 грамм гексогена при взрыве выделяют 480 кубических сантиметров газа, тогда как тротил – 285 кубических сантиметров. Иными словами, гексаген в 1.7 мощнее тротила по фугасности и динамичнее в 1,26 раза по бризантности.
Однако в СМИ чаще всего использует некий усредненный показатель. Например, атомный заряд «Малыш», сброшенный 6 августа 1945 года на японский город Хиросима, оценивают в 13-18 килотонн в тротиловом эквиваленте. Между тем это характеризует не мощность взрыва, а говорит о том, сколько необходимо тротила, чтобы выделилось столько же тепла, как и при указанной ядерной бомбардировке.
Физика горения и взрыва
2008 год, номер 4
Алюминизированные литьевые взрывчатые вещества (Обзор)
П. П. Вадхе, Р. Б. Павар, Р. К. Синха, С. Н. Астана, А. Субхананда Рао
Лаборатория исследования высокоэнергетических материалов, 411021 Пуна, Индияhemsociety@rediffmail.com
Ключевые слова: PBX, HTPB, CL-20, FOX-7, RDX, HMX, NTO, тринитротолуол, октоген, гексоген,алюминий, размер частиц, скорость детонации, малочувствительные боеприпасы, боеприпасы пониженного риска
Страницы: 98-115
Аннотация
Выполнен обзор текущего состояния и тенденций развития алюминизированных взрывчатых веществ (ВВ)
Основное внимание уделено литьевым композициям, к которым относятся как плавящиеся композиции на основе тринитротолуола (TNT), так и пастообразные композиции на основе полимеров. Детально рассмотрены хорошо изученные алюминизированные композиции на основе гексогена и октогена, в которых в качестве связующего использован TNT
Разными исследователями предложено оптимальное с точки зрения скорости детонации содержание алюминия в диапазоне 15÷20%. Однако большинство композиций имеет более высокое содержание алюминия для создания продолжительного взрывного действия, обусловленного вторичными реакциями алюминия с продуктами детонации. На параметры взрыва (скорость детонации и др.) также оказывает влияние размер частиц алюминия. В настоящее время проводятся работы с наноразмерным алюминием, полученные результаты демонстрируют неоднозначные тенденции для композиций на основе гексогена и TNT. Композиции с использованием TNT и нитротриазола служат основой для создания боеприпасов пониженного риска. Очень интересные результаты получены для композиций, содержащих динитрамид аммония и бис(2,2,2-тринитроэтил)нитрамин (BTNEN).Выявлено превосходство композиций с полимерным связующим по сравнению с традиционными ВВ на основе TNT. В частности, пластические ВВ имеют низкую уязвимость. Вообще, алюминизированные пластические ВВ нашли широкое применение в подводных приложениях. Перхлорат аммония (АР) включают в состав композиций, в частности, для усиления подводной ударной волны и энергии пузыря газообразных продуктов взрыва. В качестве связующего обычно выбирают полибутадиен с концевыми гидроксильными группами, однако исследуются и другие: нитроцеллюлоза; полиэтиленгликоль; капролактоновый полимер с энергетическими пластификаторами, например BDNPA/F; триэтиленгликольдинитрат; триметилолэтантринитрат. Композиции на основе полиэтиленгликоля и капролактона имеют низкую уязвимость, особенно при ударных воздействиях. Очень малочувствительные пластические ВВ на основе нитротриазола разрабатываются во многих странах мира. Низкочувствительная комбинация CL-20/АР отвечает требованиям высокой плотности заряда и высокой скорости детонации. Глицидилазидный полимер и полинитрометилметилоксетан, по-видимому, также представляют интерес для использования в пластических ВВ вследствие их превосходной энергетики. Однако необходимы детальные исследования чувствительности таких композиций. Представлена краткая информация о ВВ с полимерным связующим и о термобарических гелеобразных ВВ.
Взрывчатка, которая убивает своих
Наряду гексогеном и октогеном, классикой взрывчатых веществ считают трудно произносимый тетранитропентаэритрит, который чаще называют тэном. Однако из-за высокой чувствительности он так и не получил широкого применения. Дело в том, что для военных целей важна не столько взрывчатка, которая разрушительнее других, сколько – та, которая при этом не взрывается от любого прикосновения, то есть с низкой чувствительностью.
Особенно придирчиво к этому вопросы относятся американцы. Именно они разработали натовский стандарт STANAG 4439 для чувствительности взрывчатки, которая может использоваться в военных целях. Правда, это произошло уже после череды тяжелейших инцидентов, в числе которых: взрыв склада на американской базе ВВС «Бьен-Хо» во Вьетнаме, стоивший жизни 33 техникам; катастрофа на борту авианосца «Форрестол», в результате которой было повреждено 60 самолетов; детонация в хранилище авиационных ракет на борту авианосца «Орискани» (1966 года) тоже с многочисленными жертвами.
Астролит – хорош, но дурно пахнет
В начале 60-х прошлого века американская компания EXCOA презентовала новое взрывчатое вещество на основе гидразина, заявив, что оно в 20 раз мощнее тротила. Прибывших на испытания генералов Пентагона сбил с ног жуткий запах заброшенного общественного туалета. Впрочем, они были готовы его потерпеть. Однако ряд тестов с авиабомбами, заправленными астролитом А 1-5 показал, что взрывчатка оказалось лишь в два раза мощнее тротила.
После того, как чиновники Пентагона забраковали эту бомбу, инженеры из EXCOA предложили новую версию этого взрывчатого вещества уже под маркой «АСТРА-ПАК», причем для рытья окопов методом направленного взрыва. На рекламном ролике солдат тонкой струйкой поливал землю, а затем из укрытия детонировал жидкость. И окоп в человеческий рост – был готов. По своей инициативе компания EXCOA выпустила 1000 комплектов такой взрывчатки и отправила на вьетнамский фронт.
В реальности всё закончилось грустно и анекдотично. Полученные окопы источали такой отвратительный запах, что американские солдаты стремились их покинуть любой ценой, невзирая на приказы и опасность для жизни. Те же, кто оставался, теряли сознание. Неиспользованные комплекты военнослужащие за свой счет отправили назад – в офис фирмы EXCOA.
Самый мощный взрыв: Оппау, 1921 год
Вид на завод в Оппау после взрыва
Техногенная катастрофа на химическом предприятии компании BASF, расположенном близ городка Оппау, области Пфальц (Германия), стала самым мощным взрывом с участием нитрата аммония.
Взрыв прогремел 21 сентября 1921 года на заводе анилиновых красителей и удобрений. Запасы сульфата и нитрата аммония осенью не были востребованы и до весны хранились в выработанном глиняном карьере. При таком хранении они неизбежно слёживались, и на заводе использовали взрывчатку для их раздробления.
Подобный метод применялся на заводе десятки тысяч раз без всяких происшествий. Но на этот раз что-то пошло не так. По одной из версий, из-за плохого перемешивания содержание нитрата аммония в части запасов было выше обычного. По другой — подрядчик решил сэкономить и выбрал вместо чёрного пороха более мощную взрывчатку из бертолетовой соли с бензином.
Взорвалось 12 тысяч тонн смеси, в которой было около 4500 тонн нитрата аммония. Энергия взрыва оценивается в четыре-пять килотонн, а за ним последовал пожар, растянувшийся на несколько дней.
Большая часть строений в Оппау была разрушены, как и близлежащие деревни Франкенталь и Эдигхайм. Стоявшие на близлежащих станциях поезда были сброшены с путей, а в радиусе 70 километров были выбиты стёкла. Звук взрыва был слышен даже в Мюнхене — за 300 километров от Оппау.
Жертвами катастрофы стали 561 человек, и ещё больше тысячи получили ранения. Спустя десятилетия в Германии начали ходить слухи о том, что на самом деле в Оппау взорвался ядерный снаряд, придуманный немцами ещё тогда. А ещё этот взрыв попал в роман Алексея Толстого «Гиперболоид инженера Гарина».
Использование в качестве взрывчатого вещества
Воспламенение пероксида ацетона
В военных целях пероксид ацетона не используется из-за высокой летучести и чувствительности, однако, c 1980-x годов применяется в террористических целях как инициирующее или основное взрывчатое вещество. Также существуют упоминания о применении пероксида ацетона в диверсионной практике советских разведчиков первой половины 20 века как импровизированного взрывчатого вещества, которое можно легко сделать из подручных химикатов:
Использование террористами связано с простотой синтеза, а также с тем, что в молекуле данного вещества отсутствует азот, что делает невозможным определение взрывающего устройства стандартными устройствами, отвечающими на азот. Трипероксид ацетона обладает примерно такой же взрывной силой, как тротил. Кроме того, он весьма чувствителен к нагреванию и удару и может воспламеняться под действием открытого пламени и электрического разряда, что делает сам процесс создания взрывающих устройств опасным (по этой причине трипероксид ацетона получил название «Мать Сатаны»).
The Times сообщает, что через несколько дней после теракта в Манчестере (теракт произошёл в ночь на 23 мая 2017 года) в открытом доступе в социальной сети Facebook и на YouTube находились пошаговые инструкции по изготовлению взрывных устройств на основе пероксида ацетона, вещества, которое использовал Абеди для совершения теракта.
Сообщается, что данное вещество детонирует даже при содержании воды до 25 %. К удару перекись ацетона чуть менее чувствительна, чем азид свинца. По бризантности она превосходит азид свинца и гремучую ртуть.
При взрыве пероксида ацетона происходит резкое образование большого объёма газов: из его одной молекулы образуются три молекулы ацетона и одна молекула озона. Приводят также и другое уравнение разложения:
-
- (C3H6O2)3→1,3CO2+2,44CO+2,61CH4+,63C2H6+,23C2H4+,47H2+,96H2O+,47C{\displaystyle {\mathsf {(C_{3}H_{6}O_{2})_{3}\rightarrow 1,3CO_{2}+2,44CO+2,61CH_{4}+0,63C_{2}H_{6}+0,23C_{2}H_{4}+0,47H_{2}+0,96H_{2}O+0,47C}}}
Скорость детонации трипероксида ацетона составляет 5300 м/с при плотности 1,2 г/см³ и около 1430 м/с при 0,47 г/см³. В диапазоне плотностей от 0,35 до 1,2 г/см³ эта зависимость линейна и подчиняется уравнению
y=5405,1x−1149{\displaystyle y=5405,1x-1149}.
Теплота взрыва составляет 2803 кДж/кг, что составляет 67 % от тротилового эквивалента (4.19 МДж/кг)
Физико-химические свойства
Гексанитрогексаазаизовюрцитан представляет собой бесцветное кристаллическое вещество. Нерастворим в холодной воде, малорастворим в этаноле, но хорошо растворяется в ацетоне (94,6 г/100 г при 25°С), ацетонитриле, этилацетате (45,0 г/100 г при 25°С), ледяной уксусной кислоте. Сравнительно химически устойчив, однако легко разлагается гидроксидами, амидами и цианидами щелочных металлов.
Гексанитрогексаазаизовюрцитан при нормальных условиях состоит из пяти устойчивых полиморфных модификаций, которые называются α-, β-, γ-, δ- и ε-формами. Они различаются между собой пространственной ориентацией нитрогрупп, типом кристаллической решётки и числом молекул в кристаллической решётке. Эти формы способны переходить друг в друга: β-форма (орторомбическая кристаллическая ячейка) переходит в γ-форму (моноклинная кристаллическая ячейка) при 185°C, которая при нагревании до 230°C меняет свою кристаллическую структуру. α-Форму получают осаждением гексанитрогексаазаизовюрцитана хлороформом из сульфолановых растворов. δ-Форма является лабильной и существует только в условиях высокого давления. Наиболее плотной структурой и самой высокой термической устойчивостью обладает ε-форма.