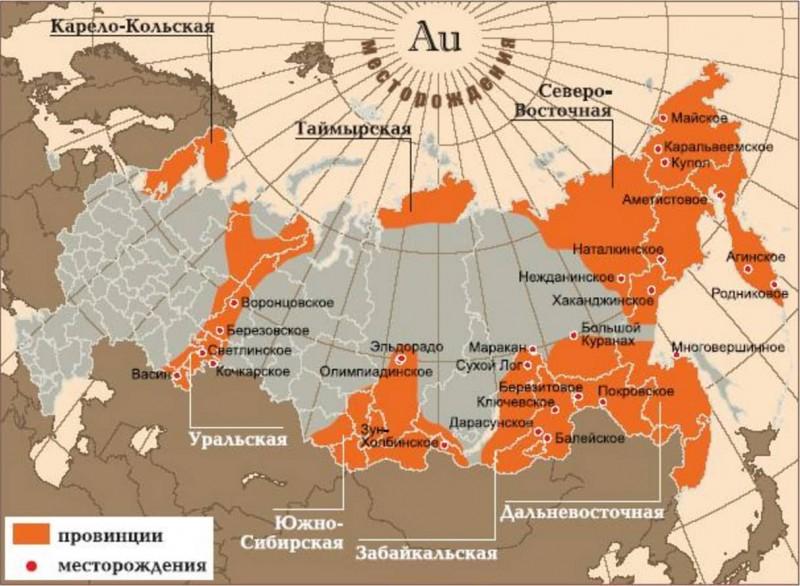
Добыча железной руды в россии, крупнейшие месторождения и способы добычи
Содержание:
Металлургия в мире
Мировая металлургия сосредоточена в 98 странах мира, из которых руда добывается только в 50. Лидерами являются пять стран — это Китай, Бразилия, Россия, Австралия и Индия, который поставляют на мировой рынок пости 80 % сырья. Большая часть мировых запасов руд — это материал среднего и низкого качества, требующий обогащения в процессе производства. Руд высокого качества в мире очень мало. Например, запасы России как одного из лидеров металлургической промышленности составляют всего 12 % от мировых запасов.
Больше всего руды добывается в Китае, а полезного железа — в России.
Лидирующими компаниями, которые регулируют мировой процесс добычи и производства руды и металлов, являются компании Arcelor Mittal, Hebei Iron & Steel, Nippon Steel.
Arcelor Mittal — это компания, образованная благодаря слиянию предприятий Индии и Люксембурга. Ей принадлежат предприятия в 60 странах мира, в том числе российское «Северсталь-Ресурс» и украинское «Криворожсталь».
Hebei Iron & Steel Group — еще одна компания, образованная в результате слияния нескольких компаний. Но вляется не частным, а государственным предприятием, зарегистрированным в Китае. Здесь производится уникальный продукт — ультратонкий холоднокатанный лист и стальные плиты. Кроме добычи и производства, компания занимается исследовательской деятельность и инвестициями.
Nippon Steel и Sumitomo Metal Industries — японский лидер по производству стали. Доменные печи этой компании были установлены еще в 1857 году.

Крупнейшие залежи
Из всех стран мира самые богатые запасы железной руды в Российской Федерации. Они сосредоточены в нескольких регионах.
Курская магнитная аномалия. Это огромный железорудный район мирового масштаба. Здесь расположено несколько мощных месторождений. Одно из них – Лебединское (14, 6 млрд т) – за свои размеры и объемы выработки дважды заносилось в книгу рекордов Гиннеса.
А также менее богатые регионы:
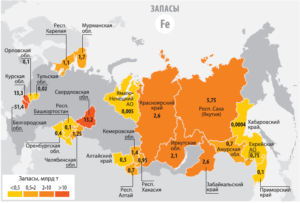 Распределение запасов железных руд
Распределение запасов железных руд
- Урал.
- Кольский рудный район.
- Карелия.
- Западная Сибирь.
Кроме России, крупные месторождения находятся на территории:
- Австралии (Айрон-Ноб, Западно-Австралийское).
- США (Верхнеозерное).
- Канады (Ньюфаундлендское, Лабрадорское).
- ЮАР (Трансваальское).
- Индии (Сингбхум).
- Швеции (гора Кирунавааре).
- Китая (возле города Аньшань).
Значительные запасы железной руды имеет Украина – более 21 млрд т. Здесь есть 3 месторождения – Криворожское, Белорецкое и Кременчугское. Последнее имеет залежи с низким содержанием железа. Кроме того, они содержат много вредных примесей. На двух других месторождениях добывается железная руда высокого качества.
Богатые железистые соединения (до 68% Fe) добывают в Венесуэле. Ресурс страны составляет 2 200 млн т. На Бразильских месторождениях Каражас, Урукум содержатся более десятка миллиардов тонн богатых залежей (50–69% Fe). Около 3 000 млн т бурого рядового железняка залегает на о. Куба.
В США находятся огромные залежи железистых кварцитов, которые требуют основательного обогащения.
 Самое крупное месторождение железной руды
Самое крупное месторождение железной руды
Уход за изделиями
Чтобы избежать порчи изделий, необходимо:
- Снимать украшения перед проведением уборки, мытьем посуды, посещением бани, сауны.
- Хранить изделия в специальном футляре или тканевом мешочке.
- В конце каждого дня снимать украшения, протирать их сухой тряпкой или салфеткой.
- Беречь изделие от попадания косметики, парфюма.
Если нужно очистить золото от налета, затемнений, можно воспользоваться домашними способами, специализированными средствами для чистки или отнести украшение в специализированную мастерскую.
Золото — драгоценный металл, применяющийся в разных сферах деятельности. Его популярность объясняется привлекательным видом, свойствами, техническими характеристиками. При добавлении других металлов можно изменить характеристики и свойства сплава.
Свойства сплавов
Свойства металлов и сплавов полностью определяются их структурой (кристаллической структурой фаз и микроструктурой). Макроскопические свойства сплавов определяются микроструктурой и всегда отличаются от свойств их фаз, которые зависят только от кристаллической структуры. Макроскопическая однородность многофазных (гетерогенных) сплавов достигается за счёт равномерного распределения фаз в металлической матрице. Сплавы проявляют металлические свойства, например: электропроводность и теплопроводность, отражательную способность (металлический блеск) и пластичность. Важнейшей характеристикой сплавов является свариваемость.
Сплавы, используемые в промышленности
Сплавы различают по назначению: конструкционные, инструментальные и специальные.
Конструкционные сплавы:
· стали
· чугуны
· дюралюминий
Конструкционные со специальными свойствами (например, искробезопасность, антифрикционные свойства):
· бронзы
· латуни
Для заливки подшипников:
· баббит
Для измерительной и электронагревательной аппаратуры:
· манганин
· нихром
Для изготовления режущих инструментов:
· победит
В промышленности также используются жаропрочные, легкоплавкие и коррозионностойкие сплавы, термоэлектрические и магнитные материалы, а также аморфные сплавы.
Мета?ллы (от лат. metallum — шахта, рудник) — группа элементов, в виде простых веществ, обладающих характерными металлическими свойствами, такими как высокие тепло- и электропроводность, положительный температурный коэффициент сопротивления, высокая пластичность и металлический блеск.
Из 118 химических элементов, открытых на данный момент (из них не все официально признаны), к металлам относят:
— 6 элементов в группе щелочных металлов,
— 6 в группе щёлочноземельных металлов,
— 38 в группе переходных металлов,
— 11 в группе лёгких металлов,
— 7 в группе полуметаллов,
— 14 в группе лантаноиды + лантан,
— 14 в группе актиноиды (физические свойства изучены не у всех элементов) + актиний, вне определённых групп бериллий и магний.
Таким образом, к металлам, возможно, относится 96 элементов из всех открытых.
В астрофизике термин «металл» может иметь другое значение и обозначать все химические элементы тяжелее гелия.
Металлургия России
В российской экономике металлургия занимает второе место после нефтегазовой промышленности. В данной сфере трудятся более 2 % работающих граждан в стране на 1,5 тыс. предприятий.
В РФ три есть основные базы черной металлургии, размещение которых объясняется близостью источников руды и бассейнов угля:
-
Уральская;
-
Сибирская;
-
Центральная.
Самое старое и крупное предприятие металлургии — Уральское, где производится половина всей продукции черной металлургии в России. Центрами Уральской металлургии являются Екатеринбург, Нижний Тагил, Челябинск и Магнитогорск. Крупнейшие предприятия — Чусовский металлургический завод и Челябинский металлургический комбинат.
Сибирская металлургическая база — самая молодая из трех и строится на смену Уральской, где исчерпаны запасы металлов практически исчерпаны. Здесь расположены всего два крупных металлургический комбината — Кузнецкий и Западно-Сибирский.
Центральная металлургическая база находится в Белгородской и Курской областях. Крупнейшим металлургическим комбинатом и заводами является Новолипецкий металлургический комбинат и заводы в Старом Осколе и Туле.
93% процента выпускаемой продукции приходится на долю шести крупных центров металлургии. Это:
-
ПАО “Северсталь”;
-
ОАО “Мечел”;
-
“Евраз”;
-
ОАО “Металлоинвест”;
-
ОАО “Новолипецкий металлургический комбинат”;
-
ОАО “Магнитогорский металлургический комбинат”.
Металлургия — промышленность, которая играет важную роль в жизни каждого человека.
Гидрометаллургия
Заключается в восстановлении металла из солевых водяных растворов. Этот технологический процесс проводится в два этапа:
- в правильно подобранном реагенте растворяют рудное соединение, которое позволяет получить раствор соли металла;
- из раствора, полученного в первом шаге, вытесняют либо активные металлы, либо проводят электролитическое восстановление.
Чтобы получить чистую медь из руды с содержанием CuO, на сырье воздействуют серной разбавленной кислотой. Из раствора сульфата методом вытеснения железа либо электролизом получают чистую медь. По аналогичной (близкой к данной методике) вырабатывают золото, уран, цинк, молибден, серебро.
Отрасли цветной металлургии
Цветная металлургия. 52 предприятия различных форм собственности. Объём товарной продукции 5,8 млрд гривен (). На собственном сырье базируется только производство титана, ферроникеля, циркония, кремния, ртути. Имеется 4 горно-обогатительных предприятий: Вольногорский государственный горно-металлургический комбинат, Иршанский горно-обогатительный комбинат, Никитовский ртутный комбинат, Побужский ферроникелевый завод. Практически все предприятия цветной металлургии значительно уменьшили объёмы производства в результате отсутствия собственной сырьевой базы, спроса на отечественном и неконкурентоспособности на мировом рынке.
Производство алюминия. Николаевский глиноземный завод (1,0 млн тонн глинозема), Запорожский производственный алюминиевый комбинат (200 тыс. тонн глинозема, 110 тыс. тонн первичного алюминия), вторичный алюминий и сплавы (158 тыс. тонн), а также строительные алюминиевые профили (15 тыс. тонн) производятся на совместных предприятиях: «Интерсплав», «Укргермет», «Обимет», Броварский завод алюминиевых строительных профилей.
Производство меди. Артемовский завод по обработке цветных металлов (прокат, сплавы, проектная мощность 140 тыс. тонн, производство в 2000 году 4,5 тыс. тонн), 9 производственно-заготовительных региональных предприятий: «Вторцветмет», СП «Донкавамет», «Укргермет», научно-производительная фирма «Форум», фирма «КАТЕХ», экспериментальный завод Государственного трубного института (город Днепр).
Производство титана и магния. Город Запорожье (Запорожский государственный титаномагниевый комбинат), производится титановая губка, шлак, ферротитан, титановое литьё.
Производство свинца и цинка. Город Константиновка («Укрцинк», выделенное предприятие «Свинец»). Практически не функционирует.
Производство полупроводников. Ранее производилось около 10 % мирового объёма, осуществлялось на 3 предприятиях: Запорожский государственный титаномагниевый комбинат, «Чистые металлы», химико-металлургическая фабрика Мариупольского металлургического комбината имени Ильича. Продукция: моно- и поликристаллический кремний, германий, арсениды и фосфиды галлия и индия, структуры и пластины на их основе.
Производство твёрдых сплавов. Относятся Светловодский казенный комбинат твердых сплавов и тугоплавких материалов, «Торезтвердосплав», Государственный инженерный центр твердых сплавов «Светкермет», концерн «Алкон» Национальной Академии наук, Государственное специализированное производственно-технологическое бюро «Инос», Государственное предприятие «ИНМА», участки различных машиностроительных заводов.
Производство углерода. Из нефтяного и пекового кокса и термоантрацита на «Укрграфит» (город Запорожье) производят угольные и графитовые электроды, блоки, анодную массу и др. Для обеспечения спецтехники на базе «Укрграфит» создан Государственный завод «Углекомпозит».
Ртутно-сурмяная промышленность. «Никитовский ртутный комбинат» (город Горловка), из-за отсутствия спроса и больших расходов прекратилось производство ртути из собственного сырья.
Производство порошковых металлов. Предприятия: Закарпатский металлургический завод, Запорожский государственный металлургический завод Института титана, Государственное предприятие «Завод порошковой металлургии» (город Бровары), «Торезтвердосплав», Светловодский казенный комбинат твердых сплавов и тугоплавких материалов, Кировский завод изделий из металлических порошков, ООО НПФ «Металлург», г. Харьков и некоторые другие предприятия чёрной металлургии.
Производство редких металлов. Вольногорский государственный горно-металлургический комбинат (гафний, цирконий), Приднепровский химический завод (цирконий, гафний и большое количество соединений редких металлов) и Мужиевский золотополиметаллический комбинат (строительство) в Закарпатской области (мощность до 60 тыс. тонн руды золота в год).
Цинк (Zn)
Главные минералы и горные породы, которые могут служить природными загрязнителями цинком, являются сфалерит, смитсонит, каламин, госларит, цинкит. Антропогенные факторы загрязнения цинком могут быть сточные воды с разных промышленных объектов (фабрики по производству минеральных красок, пергаментной бумаги, вискозного волокна и гальванические цехи).
В воде Zn находится в ионной форме, а также в форме органических и минеральных комплексов. Самыми распространёнными формами нерастворимых соединений цинка являются карбонаты, сульфиды, гидроксиды.
Содержание цинка в природных водоёмах
В морях Zn содержится в концентрациях от 1,5 до 10 мкг/литр, а в реках — 3 до 120 мкг/литр. Отходные воды с рудников и шахт, при низком рН, могут содержать очень большое количество цинка.
Zn — один из важнейших микроэлементов, в котором нуждаются все растения и животные. Есть и негативные стороны цинка, хлорид и сульфат этого элемента токсичны.
Структура металлов
Кристаллическая структура сплавов
Вакансия в кристаллической решётке
Образование дендритов
См. также: Металловедение
Ни один металл невозможно приготовить в абсолютно чистом состоянии. Технически «чистые» металлы могут содержать до нескольких процентов примесей, и если эти примеси являются элементами с низким атомным весом (например, углерод, азот или кислород), то в пересчёте на атомные проценты содержание этих примесей может быть очень большим. Первые небольшие количества примесей в металле обычно входят в кристалл в виде твёрдого раствора. Можно выделить два главных типа твёрдых растворов:
- первый, когда атомы примеси намного меньше атомов металла-растворителя, растворённые атомы располагаются в решётке растворителя по междоузлиям, или «пустотам». Образование таких твёрдых растворов — твёрдых растворов внедрения — почти всегда сопровождается расширением решётки растворителя, и в окрестности каждого растворённого атома имеется локальное искажение решётки;
- второй, когда атомы примеси и растворителя имеют приблизительно одинаковые размеры, образуется твёрдый раствор замещения, в котором атомы растворённого элемента замещают атомы растворителя, так что атомы обоих сортов занимают места в узлах общей решётки. В таких случаях тоже вокруг каждого растворённого атома имеется искажённая область, а будет ли при этом решётка расширяться или сжиматься, зависит от относительных размеров атомов растворителя и растворённого вещества.
Для большей части металлов наиболее важными элементами, образующими твёрдые растворы внедрения, являются водород, бор, углерод, азот и кислород. Присутствие дислокаций всегда приводит к появлению аномально больших или малых межатомных расстояний. В присутствии примесей каждая дислокация окружена «атмосферой» примесных атомов. Примесные атмосферы «закрепляют» дислокации, потому что в результате перемещения дислокаций будет образовываться новая конфигурация с повышенной энергией. Границы между кристаллами также являются областями с аномальными межатомными расстояниями и, следовательно, тоже растворяют примесные атомы легче, чем неискажённые области кристаллов.
При увеличении содержания примесей растворённые атомы входят и в основную массу кристалла, однако всё ещё имеется избыток примеси по границам зёрен и вокруг дислокаций. Когда содержание примеси превышает предел растворимости, появляется новая фаза, которая может представлять собой или растворённое вещество, или промежуточную фазу, или соединение. В таких случаях границы между фазами могут быть двух родов. В общем случае кристаллическая структура частичек примеси слишком отлична от структуры металла-растворителя, поэтому решётки двух фаз не могут переходить одна в другую, образуя непрерывную структуру. В таких случаях на границах раздела фаз образуются слои с нерегулярной (искажённой) структурой. С образованием границ связано появление свободной поверхностной энергии, однако энергия деформации решётки растворителя относительно невелика. В таких случаях говорят, что эти частицы выделяются некогерентно.
B ряде случаев межатомные расстояния и кристаллическая структура металла-растворителя и частичек примеси таковы, что некоторые плоскости могут соединяться между собой, образуя непрерывную структуру. Тогда говорят, что частицы второй фазы выделяются когерентно и, поскольку сопряжение решёток никогда не бывает абсолютно точным, вокруг границы образуется сильно напряжённая область. В тех случаях, когда энергия деформации слишком велика для этого, соседние кристаллы могут контактировать таким образом, что при этом в пограничных слоях возникают области упругой деформации, а на самой границе раздела — дислокации. В таких случаях говорят, что частицы выделяются полукогерентно.
При повышении температуры вследствие увеличения амплитуды колебаний атомов может образоваться дефект кристаллической решётки, который называют вакансия или «дырка». Диффузия вакансий является одним из механизмов образования дислокаций.
Как правило, кристаллизация металла происходит путём переохлаждения с образованием дендритной структуры. По мере разрастания дендритные кристаллы соприкасаются, при этом образуются различные дефекты структуры. В большинстве случаев металл затвердевает так, что первая порция кристаллов содержит меньше примесей, чем последующие. Поэтому, как правило, примеси концентрируются на границах зёрен, образуя стабильные структуры.
Добыча
Металлы получают путем извлечения из руд или вторсырья. Вся руда, содержащая ценные элементы, делится на богатую (более 55% ценных элементов), бедную (менее 50 %) и убогую (менее 25 %).
При добыче руды используются три основных метода:
-
открытый;
-
подземный;
-
комбинированный.
Открытый метод — самый распространенный и экономичный. При таком методе предприятием организуется необходимая инфраструктура и разрабатывается месторождение карьерами.
Подземный метод используется в том случае, если породы лежат глубоко под землей. По сравнению с открытым, этот метод дороже из-за необходимости специального технического оснащения. Кроме этого, он актуальнее, чем другие методы, так как запасы железной руды, залегающей близко к поверхности, практически истощены. Таким способом добывается более 70% железной руды.
Комбинированный способ, как понятно из названия, сочетает в себе два вышеуказанных метода.
Сурьма (Sb)
Главными источниками загрязнения этим элементом считаются сточные воды с предприятий, которые производят спички, стекло, краски, резину и природный процесс выщелачивания минералов сурьмы (стибиоканит, сенармонтит, стибнит, сервантит, валентинит).
Содержание сурьмы в природных водоёмах
В природных чистых водоёмах, соединения этого химического элемента не превышают норму и находятся в дисперсионном состоянии. Возможно присутствие соединений трехвалентной так и пятивалентной сурьмы.
Нормальная вода с поверхности Земли содержит очень малые концентрации сурьмы (меньше микрограмма на литр воды), в морях она содержится на уровне 0,5 мкг/литр, а в водах подземелья — около 10 мкг/литр.
Предельно-допустимая концентрация сурьмы для водной среды
В природных водоёмах максимально допустимая концентрация сурьмы (ПДКв) является 0.05 мг/литр, а в водоёмах, предназначенной для рыбохозяйственных целей (ПДКвр) — 0.01 мг/литр.
Способы добычи хрома
Разработка
Существует три способа разработки месторождений:
- открытый;
- подземный;
- комбинированный.
 Добыча хрома открытым способом
Добыча хрома открытым способом
Самым популярным способом добычи полезных ископаемых является открытый способ. Объясняется это экономичностью процесса, а также возможностью применения оборудования и техники высокой мощности. Открытый способ добычи хрома осуществляется разработкой карьеров, организовывается необходимая инфраструктура. Размеры необходимых строений определяются особенностями залежей.
Для больших глубин используется подземный метод. Способ дорогой, но позволяет осуществлять раскопки в местах, где на поверхности вести работу технически невозможно. Перед самим извлечением хрома, требуется вскрыть множество пород. Истощение запасов приводит к увеличению глубины разработки. Все чаще после извлечения руд, пустоты заполняются искусственной затвердевающей смесью.
Комбинированный способ объединяет разработку на поверхности и под землей. Они проводятся последовательно или одновременно. Экономический эффект достигается за счет наиболее полного извлечения хрома.
Примечания
- Строго говоря из-за амфотерности химических свойств полуметаллы (металлоиды) представляют собой обособленную группу, не относясь ни к металлам, ни к неметаллам; К группе металлов их можно отнести лишь условно.
- Ломоносов М. В. Основы металлургии и горного дела. — Санкт-Петербург: Императорская Академия Наук, 1763. — 416 с.
- Этимологический словарь русского языка. Вып. 10: М / Под общей редакцией А. Ф. Журавлёва и Н. М. Шанского. — М.: Изд-во МГУ, 2007. — 400 с. ISBN 978-5-211-05375-5
- (англ.) . Дата обращения 8 июня 2007.
- (англ.) . Дата обращения 8 июня 2007.
- Поваренных А. С. Твердость минералов. — АН УССР, 1963. — С. 197—208. — 304 с.
- , с. 92.
- , с. 93—94.
- , с. 97.
- , с. 103.
Классификация
Существует разделение полезных минералов, при котором они имеют вид:
- окатышей;
- агломератов;
- брикетов;
- рассыпчатой руды,
- полученной методом сепарирования.
Большое количество разнообразных по составу и происхождению минеральных ископаемых, требует распределения железных руд промышленного назначения по типам.
Магнетит-гематитовая в кварцитах. Такой минерал называют красным железняком. Залежи встречаются часто, имеют прочное строение кристаллов от вишнево-красного до красно-коричневого цвета. Поддается обработке очень сложно, имеет металлический блеск и характерную чешуйчатую или зернистую структуру.
Магно-магнетитовая в скарнах и магнетитовая руда. Структура этого минерала характерна тем, что при замещении железа на марганец, происходит увеличение структурных ячеек минерала. Может быть получена при воздействии высокой температуры в силикатной и карбонатной железных рудах.
Апатит-магнетитовый в карбонитах. Встречается со структурой кристаллов в виде иголок, призм, коротких столбцов или других форм. Часто содержит примеси различных металлов, в том числе редкоземельных элементов.
Именит-титаномагнетитовая в базитах и ультрабазитах, а также титаномагнетитовые минералы. Такой материал называют титанистым железняком, кристаллы могут иметь вид ромбоэндрических или пластинчатых форм
После извлечения теряет магнитные свойства, что очень важно для промышленной добычи.
Гетит-гидрогетитовые руды в корах выветривания. Порошкообразные, пластинчатые и игольчатые кристаллы, обычно бурого цвета, трудно поддаются плавлению паяльной лампой
Образуются под воздействием влияния атмосферных явлений.
Мартит-гидротеметитовые руды, которые образованы по кварцитам. Это минералы высокого сорта, образуются при окислении магнетита на большой глубине в гидротермальных растворах и при окислении в местах выветривания.
Применение данной классификации упрощает добычу и обработку железной руды, а также поиск полезных минералов, включающих в состав важные элементы.
Свойства
Чтобы понять, где может применяться драгоценный металл, нужно изучить его основные свойства — химические, физические, оптические, кристаллографические.
Химические
Золото — химический элемент первой группы периодической таблицы Менделеева. Его атомный номер 79. Валентность в химических соединениях — +1, +3. На золото не действует сера, кислород, но этот благородный металл не является инертным. При нагревании до 700°C на поверхности образуется оксидная пленка, которая при дальнейшем нагреве не разрушается в течение 12 часов.
Физические
Свойства:
- Цвет — бело-желтый с серебристыми прожилками или насыщенный желтый.
- Прозрачность — непрозрачный материал.
- Блеск — присутствует.
- Плотность — до 19,3 г/см3.
- Показатель твердости по шкале Мооса — до 3.
- Радиоактивность — 0.
Оптические
Свойства:
- Тип — изотропный.
- Цвет в отраженном свете — красноватый или желтый, который переходит в белый.
- Благородный металл не флуоресцентный.
- Золото не плеохроирует.
Кольца из красного и белого золота (Фото: Instagram / dreams_krsk)