Определение функции эндотелия
Содержание:
- Классификация
- Что такое эпителиальные клетки
- Что такое эндотелий — «тефлон» наших сосудов?
- Здоровый эндотелий — здоровые сосуды
- Строение специализированных форм эндотелия
- Эндотелиальная клетка
- Стенки кровеносных сосудов, эндотелий. Эндотелий сосудов. Роль эндотелия в регуляции просвета сосудов Из одного слоя клеток эндотелия состоят
- Что такое мезотелий
- Гормоны сосудов. Гормоны эндотелия. Эндотелин. Регуляторная функция гормонов сосудистого эндотелия. Эндотелиалъный гиперполяризующий фактор.
- Диагностика эндотелиальной дисфункции сосудов
- Антикоагуляционные свойства эндотелия сосудов
- Эндотелиальные клетки, клетки купфера и ито
- Альтернативная классификация
Классификация
Наиболее важную роль в организме человека играет белок семейства VEGF, называемый VEGF-A. В данное семейство также входят плацентарный фактор роста (PGF) и белки VEGF-B, VEGF-C, VEGF-D. Все они были обнаружены позже, чем VEGF-A (до их обнаружения белок VEGF-А назывался просто VEGF).
Наряду с перечисленными были открыты белок VEGF, кодируемый вирусами (VEGF-E), и белок VEGF, содержащийся в яде некоторых змей (VEGF-F).
| Тип | Функция |
|---|---|
| VEGF-A |
|
| VEGF-B | Эмбриональный ангиогенез (в частности, тканей миокарда) |
| VEGF-C | Ангиогенез лимфатических сосудов |
| VEGF-D | Развитие лимфатических сосудов в лёгких |
| PIGF | Васкулогенез (а также ангиогенез при ишемии, воспалении, заживлении ран и раке) |
Активность белка VEGF-А изучалась (как следует из его названия) в основном на клетках эндотелия сосудов, хотя он оказывает влияние на функционирование и других типов клеток (например, стимулирует миграции моноцитов/макрофагов, действует на нейроны, клетки раковых опухолей, почечные эпителиальные клетки). В исследованиях in vitro было показано, что VEGF-A стимулирует митогенез эндотелиальных клеток и их миграции. VEGF-A также усиливает и увеличивает проницаемость микрососудов и был первоначально назван «Сосудистый фактор проницаемости».
Что такое эпителиальные клетки
Эпителиальные клетки относятся к любому типу животных клеток, которые покрывают поверхности или выстилают полость, выполняя секреторные, транспортные или регуляторные функции. Апикальная базальная полярность является одной из основных характеристик эпителия. Это означает, что базальная поверхность эпителиальных клеток прикреплена к базальной пластинке, а апикальная поверхность клеток обращена к просвету. Эпителиальные клетки располагаются вместе, чтобы создать непрерывный лист, формируя десмосомы и плотные соединения. Базальная пластинка прикреплена к слою соединительной ткани, называемой сетчатой пластинкой. Кровоснабжение между эпителиальными клетками (аваскулярными) не обнаружено. Более того, в нем нет нервной системы (иннервируется). Эпителиальные клетки также обладают высокой регенеративной способностью. Эпителиальные клетки показаны на фиг.1 .
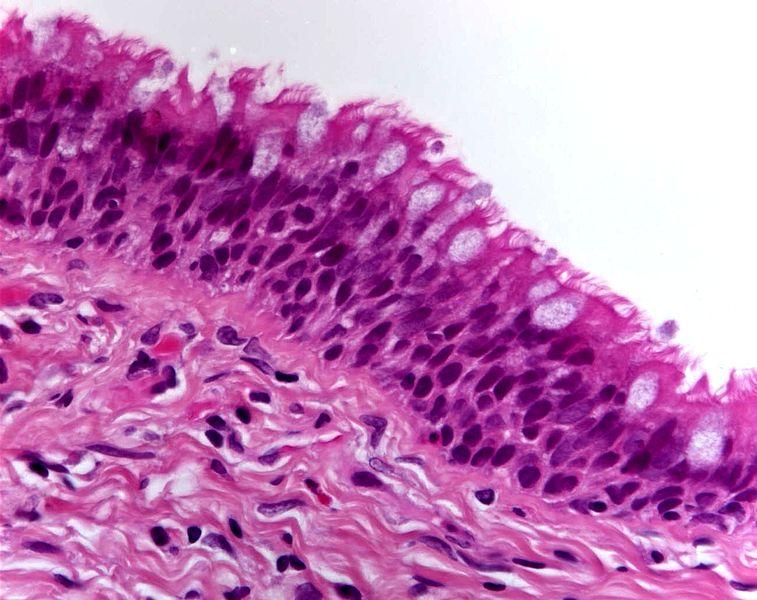
Рисунок 1: Эпителиальные клетки
Три типа клеток встречаются в эпителии. Они плоские, кубовидные и столбчатые. Сквамозный эпителий состоит из плоских и чешуйкообразных клеток. Кубоидальные клетки похожи на блоки, а столбчатые клетки высокие. Эти три типа ячеек либо расположены в один слой клеток, либо в несколько слоев клеток. Когда эпителий состоит из одного слоя эпителиальных клеток, он называется простым эпителием. С другой стороны, несколько слоев эпителиальных клеток продуцируют многослойный эпителий.

Рисунок 2: Расположение и функция эпителиальных клеток
Псевдостратифицированный эпителий является альтернативным типом эпителия, высота клеток которого варьируется. Переходный эпителий — это другой тип эпителия, который позволяет растягивать мочевые органы. Некоторые эпителиальные клетки содержат проекции и реснички. Тип, расположение и функция эпителиальных клеток показаны на рисунке 2 .
Что такое эндотелий — «тефлон» наших сосудов?
Эндотелий представляет собой внутреннюю выстилку кровеносных сосудов, отделяющую кровоток от более глубоких слоев сосудистой стенки. Это непрерывный монослой (1 (!) слой) эпителиальных клеток, формирующих ткань, масса которой составляет у человека 1,5-2,0 кг. Эндотелий непрерывно вырабатывает огромное количество важнейших биологически активных веществ, являясь, таким образом, гигантским паракринным органом, распределенным по всей площади человеческого организма.
Функции эндотелия
Эндотелий сосудов выполняет множество различных функций, в том числе и важнейшую барьерную функцию. Он является первым и последним рубежом, где решается судьба наших сосудов. Это он «даёт пинка» всему, чему не место в стенке сосуда. И наоборот, если он «сломался», в стенку лезут нежелательные гости, и там начинается тихое безобразие, которое заканчивается инфарктом.
В контексте этой статьи для нас важно, что все факторы риска развития сосудистых заболеваний, будь то курение, высокий уровень хлестерина или малоподвижный образ жизни, «бьют» в эндотелий, и если он пока «терпит» — что ж, продолжайте в том же духе — вам повезло с наследственностью, а если он дал сбой — вам нужно менять свою жизнь. Также ключевая функция эндотелия состоит в регуляции тонуса сосудов, процессов адгезии лейкоцитов и баланса профибринолитической и протромбогенной активности
Решающую роль при этом играет образующаяся в эндотелии окись азота (NO). Монооксид азота выполняет важную функцию в регуляции коронарного кровотока, а именно, расширяет или сужает просвет сосудов в соответствии с потребностью организма
Также ключевая функция эндотелия состоит в регуляции тонуса сосудов, процессов адгезии лейкоцитов и баланса профибринолитической и протромбогенной активности. Решающую роль при этом играет образующаяся в эндотелии окись азота (NO). Монооксид азота выполняет важную функцию в регуляции коронарного кровотока, а именно, расширяет или сужает просвет сосудов в соответствии с потребностью организма.
Увеличение тока крови, например, при физической нагрузке, благодаря усилиям протекающей крови приводит к механическому раздражению эндотелия. Это механическое раздражение стимулирует синтез NO. Если эндотелий способен производить NO, значит он здоров, и его функция не нарушена.
Эндотелиальная дисфункция
При повреждении эндотелия равновесие нарушается в сторону сосудосужения. Это неравновесие между сосудорасширением и сосудосужением характеризует состояние, которое называют дисфункцией эндотелия.
Сужение, стеснение сосудов называется стеноз. Стенозирование происходит из-за «бляшек», образующихся на стенках сосудов. Подобная бляшка — это тромб — патологический сгусток крови в просвете кровеносного сосуда или в полости сердца. Помимо обычной угрозы эндотелиальной дисфункции, срыв этих «бляшек» приводит к таким страшным проявлениям атероскероза, как инфаркт, инсульт и пр.
Заболевания, связанные с эндотелиальной дисфункцией:
- атеросклероз,
- гипертоническая болезнь,
- коронарная недостаточность,
- инфаркт миокарда,
- диабет и инсулинорезистентность,
- почечная недостаточность,
- наследственные и приобретенные нарушения обмена (дислипидемия и др.),
- тромбоз и тромбофлебит
- эндокринные возрастные нарушения,
- не дыхательные легочные патологии (астма)
Технология АнгиоСкан применительно к эндотелиальной функции основана на регистрации изменений параметров пульсовой волны, происходящих после проведения теста с окклюзией плечевой артерии, т.е. на пульсовой диагностике. В течении 1 минуты после 5 минутного пережатия артерии мы заставляем эндотелий работать, и оцениваем то как он справляется со своей функцией расширения сосудов (вазодилатацией).
Здоровый эндотелий — здоровые сосуды
Новый ангиопротектор ЛонгаДНК (патент №2338541) – оптимальное сочетание нутриентов для улучшения функционального состояния эндотелия сосудов и восстановления организма.
Зачем же нужно «поддерживать» эндотелий?
Эндотелий — активный эндокринный орган. Он регулирует процесс свертывания крови, тонус сосудов и артериальное давление. Именно эндотелий, выделяя NO, обеспечивает расширение сосудов. Это открытие было удостоено Нобелевской премии в 1998 году.
Эндотелий прорастает в поврежденные патологическим процессом части органов, формирует там новые капилляры и запускает процесс восстановления органа после болезни. Чем лучше работает эндотелий, тем лучше восстанавливается орган после болезни, и тем >меньше мы стареем. Старят не годы – болезни!
ЛонгаДНК создана для поддержки эндотелия сосудов. Для достижения надежного результата доктор Шубин А.И. рекомендует 3-4 30-дневных курса приема ЛонгаДНК в течение года.

Упаковка из 30 капсул рассчитана на минимально рекомендованный курс приема — 15 дней.
ГР: 77.99.23.3.У.12426.10.06 от 17/11/2006, Юсерп (Россия), производство В-МИН; НД: ТУ 9253-002-49888681-06
Срок хранения: 3 года; Условия хранения: В сухом, защищенном от света месте, при температуре не выше 250С.
L-аргинин – аминокислота, основной источник для образования оксида азота (NO) в клетках эндотелия сосудов, нервных клетках и макрофагах. NO играет главную роль в процессе расслабления гладкой мышцы сосудов, что приводит к снижению артериального давления, препятствует образованию тромбов. Огромное значение NO имеет для нормального функционирования нервной и иммунной систем.
На сегодняшний день экспериментально и клинически доказаны следующие эффекты L-аргинина:
- Один из самых эффективных стимуляторов продукции соматотропного гормона гипофиза (гормона роста), позволяет поддерживать его концентрацию на верхних границах нормы, что способствует улучшению настроения, делает человека более активным, инициативным и выносливым; все долгожители имеют повышенный уровень гормона роста;
- Увеличивает скорость восстановления поврежденных тканей – ран, растяжений сухожилий, переломов костей;
- Увеличивает мышечную и уменьшает жировую массу тела, эффективно помогая похудеть;
- Эффективно усиливает сперматогенез, что используется для лечения бесплодия у мужчин;
- Играет существенную роль в процессах запоминания новой информации;
- Является гепатопротектером, улучшающим функции печени;
- Стимулирует активность макрофагов, защищающих организм от агрессии чужеродных бактерий.
ДНК – дезоксирибонуклеиновая кислота – источник нуклеотидов для синтеза собственной ДНК в активно размножающихся клетках (эпителий желудочно-кишечного тракта, клетки крови, клетки эндотелия сосудов):
- Мощно стимулирует клеточную регенерацию и восстановительные процессы, ускоряет заживление ран;
- Обладает выраженным иммуномодулирующим эффектом, усиливает фагоцитоз и местный иммунитет, за счет чего резко повышает устойчивость и невосприимчивость организма к инфекциям; обладает антиаллергическим действием;
- Восстанавливает адаптационные возможности органов, тканей и организма человека в целом.
Строение специализированных форм эндотелия
Эндотелиоцитам соматического или закрытого типа характерны плотные щелевые контакты, реже — десмосомы. На периферических участках такого эндотелия толщина клеток составляет 0,1-0,8 мкм. В их составе можно заметить многочисленные микропиноцитозные везикулы (органоиды, запасающие полезные вещества) непрерывной базальной мембраны (клеток, отделяющих соединительные ткани от эндотелия). Этот вид эндотелиальных клеток локализуется в железах внешней секреции, центральной нервной системе, сердце, селезенке, легких, и крупных сосудах.
Для фенестрированного эндотелия характерны тонкие эндотелиоциты, в которых присутствуют сквозные диафрагмированные поры. Плотность в микропиноцитозных везикулах очень мала. Также присутствует непрерывная базальная мембрана. Чаще всего встречаются такие эндотелиальные клетки в капиллярах. Клетки такого эндотелия выстилают капиллярные русла в почках, эндокринных железах, слизистых оболочках пищеварительных путей, сосудистых сплетениях мозга.
Главным отличием синусоидного типа эндотелиальных клеток сосудов от остальных является то, что их межклеточные и трансцеллюлярные каналы очень крупные (до 3 мкм). Характерна прерывистость базальной мембраны либо ее полное отсутствие. Такие клетки присутствуют в сосудах головного мозга (они участвуют в транспортировке форменных элементов крови), коре надпочечных желез и печени.
Решетчатые клетки эндотелия представляют собой палочковидные (либо веретеновидные) клетки, которые окружает базальная мембрана. Они также принимают активное участие в миграции клеток крови по организму. Местом их локализации являются венозные синусы в селезенке.
В состав ретикулярного типа эндотелия входят звездчатые клетки, которые переплетаются с базолатеральными отростками цилиндрической формы. Клетки этого эндотелия обеспечивают транспортировку лимфоцитов. Они входят в состав сосудов, проходящих через органы иммунной системы.
Эндотелиальные клетки, которые находятся в лимфатическом русле, являются самыми тонкими из всех типов эндотелия. Они содержат повышенный уровень лизосом и в их состав входят более крупные везикулы. Базальной мембраны вообще нет, либо она прерывистая.
Существует также особый эндотелий, который выстилает заднюю поверхность роговицы человеческого глаза. Эндотелиальные клетки роговицы транспортируют в нее жидкость и растворенные вещества, а также поддерживают ее дегидрированное состояние.
Эндотелиальная клетка
Эндотелиальные клетки не только восстанавливают выстилку существующих кровеносных сосудов, но и создают новые сосуды. Это обязательно должно происходить у зародыша, чтобы сосудистая сеть не отставала от роста тела, и в тех тканях взрослого организма ( кость, стенка матки), которые подвергаются циклическим перестройкам, а также при заживлении повреждений.
Эндотелиальные клетки образуют одиночный слой, выстилающий все кровеносные сосуды и регулирующий обмен веществами между кровью и окружающими тканями. Новые кровеносные сосуды развиваются из стенок существующих мелких сосудов в виде выростов эндотелиалъных клеток; эти клетки способны образовывать полые капиллярные трубочки даже при росте в культуре. В живом организме поврежденные ткани и некоторые опухоли обеспечивают себе кровоснабжение, выделяя вещества, которые стимулируют образование новых капиллярных веточек близлежащими эндотелиальными клетками. Рост опухолей, не способных вызвать такую реакцию эндоте-лиальных клеток, быстро прекращается.
Эндотелиальные клетки, выстилающие внутреннюю поверхность кровеносных сосудов, имеют постоянный контакт с циркулирующим пулом клеток крови.
Эндотелиальные клетки секретируют во внешнюю среду GM-CSF, IL-1, 6, 7, TNFa, хемокины и другие вещества, играющие роль инициаторов и регуляторов иммунных реакций.
|
Юкстаканаликулярная ткань в глазу с начальной простой глаукомой. |
Эндотелиальные клетки внутренней стенки синуса не имеют выраженной базальной мембраны. Они лежат на очень тонком неравномерном слое волокон ( преимущественно эластических), связанных основной субстанцией. Короткие эндоплазматические отростки клеток проникают в глубь этого слоя, что увеличивает прочность их соединения с юкстаканаликулярной тканью.
Распад эндотелиальных клеток и перицитов расценивается в качестве неспецифического эффекта при дегенерациях, ретинопа-тиях и окклюзии сосудов. Ацелюлярные капилляры легко запу-стевают, циркуляция крови в них прекращается.
Паразитируют в красных кровяных и эндотелиальных клетках человека и животных ( млекопитающих, птиц и пресмыкающихся); весь жизненный никл проходит внутри тела хозяина.
Интересно, что эндотелиальные клетки в результате активации тоже могут продуцировать окись азота во внеклеточную среду.
Простациклины образуются в эндотелиальных клетках эндокарда и сосудов. Они препятствуют агрегации тромбоцитов; расширяют коронарные сосуды и снижают давление крови, действуя на гладкие мышцы сосудов.
Во всей сосудистой системе взрослого организма эндотелиальные клетки сохраняют способность к делению и передвижению. Если, например, участок стенки аорты будет поврежден и лишится своей эндотелиальной выстилки, в окружающем эндотелии образуются новые клетки, которые перемещаются так, чтобы покрыть поврежденное место. Новые клетки способны даже покрывать внутреннюю поверхность пластиковых трубок, используемых хирургами для замещения поврежденных частей кровеносных сосудов.
|
Опухолевая ткань, пересаженная в роговицу, выделяет фактор, вызывающий прорастание в опухоль капилляров. Капилляры обеспечивают опухоль питательными веществами из общего кровотока, и это позволяет ей расти. Процесс образования капилляров называется ангиогене-зом. |
Такого рода наблюдения показывают, что эндотелиальные клетки, которые в будущем сформируют новый капилляр, отрастают от стенки существующего капилляра или небольшой венулы, выпуская сначала псевдоподии ( рис. 16 — 17); затем образуется толстый отросток, который позже становится полым и превращается в трубку. Первый признак образования такой трубочки в культуре-это появление в клетке удлиненной вакуоли, которая вначале полностью окружена цитоплазмой. Такие же вакуоли возникают в соседних клетках, и в конце концов клетки выстраивают свои вакуоли концом к концу так, что эти вакуоли сливаются в один непрерывный канал. Капилляры, образующиеся в чистой культуре эндотелиальных клеток, не содержат крови, и по ним не протекает никакая жидкость. Очевидно, что ток и давление крови не нужны для образования капиллярной сети.
Новый кровеносный капилляр образуется путем отпочковывания эндотелиальной клетки от стенки существующего малого сосуда. Эта схема основана на наблюдениях над клетками в прозрачном хвосте живого головастика.
|
Нарушение проницаемости стенки сосудов сетчатки, экстравазаль-ная флюоресценция у больного препролиферативной диабетической ретинопатией. Флюоресцентная ангиограмма, поздняя венозная фаза. |
Стенки кровеносных сосудов, эндотелий. Эндотелий сосудов. Роль эндотелия в регуляции просвета сосудов Из одного слоя клеток эндотелия состоят

Человеческий организм состоит из множества различных клеток. Из одних состоят органы и ткани, а из других – кости. В строении кровеносной системы человеческого организма огромную роль играют эндотелиальные клетки.
Классификация капилляров
Поструктурно-функциональным особенностямразличают три типа капилляров:соматический, фенестрированный исинусоидный, или перфорированный.
Наиболеераспространенный тип капилляров –соматический.В таких капиллярах сплошная эндотелиальнаявыстилка и сплошная базальной мембраной.Капилляры соматического типа находятсяв мышцах, органах нервной системы, всоединительной ткани, в экзокринныхжелезах.
Второйтип – фенестрированныекапилляры.Они характеризуются тонким эндотелиемс порами в эндотелиоцитах. Поры затянутыдиафрагмой, базальная мембрана непрерывна.Фенестрированные капилляры встречаютсяв эндокринных органах, в слизистойоболочке кишки, в бурой жировой ткани,в почечном тельце, сосудистом сплетениимозга.
1 – эндотелиоцит;2 – базальная мембрана; 3 – фенестры; 4- щели (поры); 5 – перицит; 6 – адвентициальнаяклетка; 7 – контакт эндотелиоцита иперицита; 8 – нервное окончание.
Что такое мезотелий
Мезотелий — это эпителий, который выстилает брюшину, перикард и плевру. Мезотелиальные клетки происходят из мезодермы. Брюшина — это серозная оболочка, которая выстилает брюшную полость. Висцеральная брюшина и теменная брюшина являются двумя категориями брюшины. Висцеральная брюшина выравнивает внутренние органы, тогда как париетальная брюшина выравнивает тазовую и брюшную полости. Оба типа брюшины выстланы мезотелиальными клетками. Перикард — это слизистая оболочка сердца и средостение, Средостение — это область между легкими. Плевра — это слизистая оболочка легких. Висцеральная плевра и париетальная плевра — это два типа плевры. Висцеральная плевра лежит непосредственно над легкими, тогда как теменная плевра — это наружный слой легких.

Рисунок 1: Мезотелиальные клетки
Основная функция мезотелия в брюшине, перикарде и плевре заключается в обеспечении скользкой, но не липкой поверхности между органами, защищая органы в грудной клетке и животе и обеспечивая функционирование органов. Помимо этого, мезотелий позволяет движение жидкостей и веществ между внутренними органами и внешней средой. Это также помогает в свертывании крови и заживлении тканей. Мезотелий также играет иммунологическую роль против инфекций и образования опухолей. Мезотелиома, спайки, фиброз и плевральные выпоты являются общими осложнениями мезотелия.
Гормоны сосудов. Гормоны эндотелия. Эндотелин. Регуляторная функция гормонов сосудистого эндотелия. Эндотелиалъный гиперполяризующий фактор.
Клетки сосудистого эндотелия синтезируют и выделяют через апикальную и базальную мембраны три группы гормонов: сосудосуживающие (эндотелины, тромбоксаны), сосудорасширяющие (оксид азота, гиперполяризующий фактор, простагландины) и факторы адгезии и агрегации клеточных элементов.
Эндотелины (ЭТ) являются крупными полипептидами (21 аминокислота), образуются путем частичного гидролиза молекулы предшественника или «большого эндотелина», состоящей из 38 аминокислот, под влиянием связанного с мембраной клетки и находящегося в цитоплазматических везикулах эндотелинпревращающего фермента. Этот фермент локализован в эндотелии сосудов легких, сердца, почек, плаценты, поджелудолчной железы, надпочечников, головного мозга и даже в сосудистых гладких мышцах. Наличие двух форм эндотелинпревращающего фермента (мембрано-связанной и внутриклеточной) определяет и два места образования эндоте-линов — в цитоплазме и на поверхности клеточной мембраны. Эндотелин-превращающий фермент ведет не только к образованию молекул эндотелина, но способен вызывать гидролиз и инактивацию на поверхности эн-дотелиоцитов ряда регуляторных пептидов и гормонов (инсулина, бради-кинина, нейротензина и др.). Активация эндотелинпревращающего фермента происходит под влиянием цитокинов.

Эффекты эндотелинов обусловлены их взаимодействием со специфическими мембранными рецепторами двух типов — ЭТ-А и ЭТ-В. Следствием специфического связывания эндотелина с рецептором является активация систем вторичных посредников (фосфолипаза С, ИФЗ, диацилглицерол, цГМФ и цАМФ, фосфолипазы D и А2). Различают прямые и опосредованные сосудистые эффекты эндотелинов. Прямые эффекты заключаются в действии на гладкие мышцы сосудов. Связывание эндотелина с рецепторами гладких мышц сосудов вызывает их сокращение и вазоконстрикцию (через образование ИФЗ и повышение внутриклеточного Са2+), а также стимуляцию митогенеза и пролиферации клеток (через активацию тирозинкиназы и фосфорилирование тирозина). Взаимодействие эндотелинов с рецепторами клеток эндотелия вызывает реализацию опосредованных эффектов, в виде высвобождения из эндотелия вазоактивных факторов, приводящих к расширению сосудов (N0, гиперполяризующий фактор, простагландины). Кроме сосудистых эффектов эндотелины изменяют секрецию гормонов гипофиза и надпочечников, стимулируют секрецию атрио-пептида миокардом, угнетают эффекты вазопрессина в почках, способствуя диурезу и натрийурезу, увеличивают реакции сердца на симпатические стимулы.
Среди сосудорасширяющих гормонов эндотелия основное место по выраженности и распространенности эффекта занимает оксид азота (N0), постоянно образующийся из L-аргинина под влиянием фермента NO-син-тетазы. Одним из стимулов, активирующих фермент и образование оксида азота, является механическое растяжение стенки сосудов. Активация фермента и синтез оксида азота происходят при действии на мембранные рецепторы эндотелиоцитов ацетилхолина, адреномедуллина, гистамина, брадикинина, АТФ, а также в результате повышения в клетке эндотелия концентрации ионизированного Са2+. NO-синтетаза помимо образования оксида азота стимулирует синтез некоторых цитокинов: интерлейкина — 1(3, альфа-интерферона, тогда как другие цитокины: ИЛ-4, ИЛ-8, ИЛ-10, напротив, подавляют активацию фермента.
Вазодилатирующий эффект N0 опосредуется активацией образования в гладкомышечных клетках цГМФ. Оксид азота также подавляет вазоконстрикторное действие ангиотензина-II. Синтезированный клетками эндотелия оксид азота выделяется не только через базальную мембрану в сторону гладкомышечных клеток кровеносных сосудов, но и через апикальную мембрану, где тормозит адгезию тромбоцитов и лейкоцитов крови к эндо-телиальной выстилке стенки сосуда. Антиагрегантное действие оксида азота отчасти опосредовано простациклином, образующимся в эндотелии.
В нервной системе N0 является модулятором синаптической передачи, так как выявлено его поступление в синаптическую щель и показано инги-бирующее влияние на выделение медиаторных аминокислот.
Эндотелиалъный гиперполяризующий фактор также вызывает дилатацию артериальных и венозных сосудов, но отличается от N0 механизмом действия — способностью активировать ионные каналы (К+,Сl) и снижать возбудимость эндотелиальных клеток.
К числу факторов регуляции адгезии и агрегации клеток относятся многочисленные интегрины и селектины, образуемые клетками эндотелия.
Диагностика эндотелиальной дисфункции сосудов
Своевременное выявление данного недуга позволяет предотвратить и «последующие» болезни, вплоть до инфаркта
Очень важно вычислить сосудистый участок, на котором эндотелий дисфункционален. Состояние эндотелия на данном участке (например, в коронарных сосудах или в артерии) может быть проверено ангиограммой или ультразвуковыми исследованиями
В обоих случаях пациенту назначают прием сосудорасширяющих препаратов (как правило, ацетилхолин).
Еще один метод диагностики: измерение «времени передачи пульса» (Pulswellenlaufzeit, также pulsetransittime, или PTT) – важного кардиоваскулярного показателя, отражающего, в частности, степень эластичности сосудов. Если выявляется недостаточная эластичность, это может указывать среди прочего и на эндотелиальную дисфункцию
Обычно время передачи пульса устанавливается на участке от сердца до указательного пальца. Начало пульса (сокращение сердечной мышцы) регистрируется на электрокардиограмме. При этом учитываются ЭКГ-максимумы, так называемые R-зубцы. А момент «добегания волны пульса» до указательного пальца фиксируется пульсоксиметром, который, вообще говоря, применяется для определения насыщения крови кислородом («прищепка», прицепленная к указательному пальцу пациента, являющаяся спектрофотометрическим датчиком).
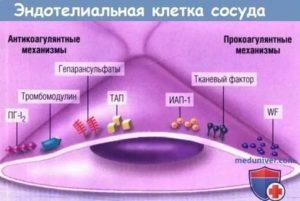
Антикоагуляционные свойства эндотелия сосудов
Антикоагулянты — это вещества, понижающие свертываемость крови. Выделяемые эндотелием, они, так сказать, действуют в трех направлениях:
Первое: подавление тромбоцитов. Тромбоциты – особые клеточные фрагменты, лишенные ядер. Они постоянно присутствуют в крови и реагируют на повреждение сосудов, из-за которых возникают кровотечения. В этом случае они формируют клеточный агрегат (первичную пробку), который закрывает место повреждения сосуда. Однако поверхность тромбоцитов может быть использована для ускорения неконтролируемой реакции плазменного свертывания, без повреждения сосудов. Таким образом, тромбоциты, способствуя остановке кровотечений, могут способствовать и развитию тромбоза.
Выделяемые эндотелием вещества, которые подавляют активность тромбоцитов:
- простациклин (простагландин I2);
- оксид азота;
- эктонуклеатидаза.
Второе: понижение свертываемости. Этому способствуют следующие продукты эндотелия:
- протеин С;
- гепарансульфат, запускающий процесс синтеза антитромбина в крови;
- ингибитор фактора свертываемости крови (замедляет действие белково-фосфолипидного комплекса, который называется фактор свертывания крови III).
Третье: поддержка фибринолиза. Процесс разложения тромбов в крови называется фибринолизом. Этот процесс предотвращает закупорку сосудов фибрином, неглобулярным белком, принимающим в плазме форму волокон, которые образуют «скелет» формирующегося тромба. Таким образом фибринолиз – это лишение тромбов их «скелета», в результате чего прекращается и сам процесс образования тромбов. Вещества, способствующие фибринолизу:
- тканевые активаторы плазминогена (t-PA, u-PA);
- аннексины.
Эндотелиальные клетки, клетки купфера и ито
Строение эндотелиальных клеток, клеток Купфера и Ито, мы рассмотрим на примере двух рисунков.
На рисунке справа от текста, изображены синусоидные капилляры (СК) печени — внутридольковые капилляры синусоидного типа, увеличивающиеся от входных венул к центральной вене. Печеночные синусоидные капилляры формируют анастомотическую сеть между печеночными пластинками. Выстилка синусоидных капилляров образована эндотелиальными клетками и клетками Купфера.
На рисунке слева от текста, изображена печеночная пластинка (ПП) и два синусоидных капилляра (СК) печени срезаны вертикально и горизонтально, чтобы показать перисинусоидальные клетки Ито (КИ). На рисунке отмечены также срезанные желчные канальцы (ЖК).
ЭНДОТЕЛИАЛЬНЫЕ КЛЕТКИ
Эндотелиальные клетки (ЭК) — сильно уплощенные чешуйчатые клетки с удлиненным маленьким ядром, слаборазвитыми органеллами и большим количеством микропиноцитозных везикул. Цитомембрана испещрена непостоянными отверстиями (О) и фенестрами, часто группирующимися в решетчатые пластинки (РП).
Эти отверстия пропускают плазму крови, но не клетки крови, давая ей возможность доступа к гепатоцитам (Г). Эндотелиальные клетки не имеют базальной мембраны и не обладают фагоцитозом. Они соединены друг с другом с помощью небольших соединительных комплексов (не показаны).
Вместе с клетками Купфера эндотелиальные клетки формируют внутреннюю границу пространства Диссе (ПД); его наружная граница образована гепатоцитами.
КЛЕТКИ КУПФЕРА
Клетки Купфера (КК) — большие, непостоянные звездчатые клетки внутри печеночных синусоидных капилляров, частично на их бифуркациях.
Отростки клеток Купфера проходят без каких-либо соединительных устройств между эндотелиальными клетками и часто пересекают просвет синусоидов.
Клетки Купфера содержат овальное ядро, много митохондрий, хорошо развитый комплекс Гольджи, короткие цистерны гранулярной эндоплазматической сети, множество лизосом (Л), остаточные тела и редкие кольцевые пластинки. Клетки Купфера также включают большие фаголизосомы (ФЛ), которые часто содержат отжившие свой срок эритроциты и инородные вещества.
Также могут быть выявлены, особенно при суправитальной окраске, включения гемосидерина или железа.
Поверхность клеток Купфера демонстрирует непостоянные уплощенные цитоплазматические складки, называемые ламеллоподиями (ЛП) — пластинчатыми ножками, а также отростки, называемые филоподиями (Ф), и микроворсины (Мв), покрытые гликокаликсом. Плазмолемма формирует червеобразные тельца (ЧТ) с центрально расположенной плотной линией. Эти структуры могут представлять конденсированный гликокаликс.
Клетки Купфера — это макрофаги, весьма вероятно, формирующие самостоятельный род клеток. Они обычно происходят от других клеток Купфера вследствие митотического деления последних, но могут также происходить из костного мозга. Некоторые авторы полагают, что они являются активизированными эндотелиальными клетками.
Иногда случайное автономное нервное волокно (НВ) проходит через пространство Диссе. В некоторых случаях волокна имеют контакт с гепатоцитами. Края гепатоцитов отграничены межгепатоцитными углублениями (МУ), усеянными микроворсинками.
КЛЕТКИ ИТО
Это звездчатые клетки, локализованные внутри пространств Диссе (ПД). Ядра их богаты конденсированным хроматином и обычно деформированы большими липидными каплями (ЛК). Последние присутствуют не только в перикарионе, но и в отростках клетки и видимы снаружи как сферические протрузии.
Органеллы развиты плохо. Перисинусоидальные клетки демонстрируют слабую эндоцитотическую активность, но не обладают фагосомами. Клетки имеют несколько длинных отростков (О), которые контактируют с соседними гепатоцитами, но не образуют соединительных комплексов.
Отростки охватывают синусоидные капилляры печени и в некоторых случаях проходят через печеночные пластинки, вступая в контакт с соседними печеночными синусоидами. Отростки не постоянны, разветвлены и тонки; они могут быть также уплощенными.
Накапливая группы липидных капель, они удлиняются и приобретают вид виноградной кисти.
Считается, что перисинусоидальные клетки Ито — это слабодифференцированные мезенхимные клетки, которые могут рассматриваться как гемопоэтические стволовые клетки, так как они могут в патологических условиях трансформироваться в жировые клетки, активные кровяные стволовые клетки или в фибробласты.
Альтернативная классификация
Понятие «белков VEGF» — широкое понятие, охватывающее две группы белков, которые возникают в результате альтернативного сплайсинга матричной РНК (мРНК) одного гена, содержащего 8 экзонов. Эти две группы различаются сайтом сплайсинга терминального 8-го экзона: белки с проксимальным сайтом обозначаются как VEGFxxx, а с дистальным — как VEGFxxxb. Кроме того, альтернативный сплайсинг 6-го и 7-го экзонов изменяет их гепарин-связывающие свойства и аминокислотный состав (у людей: VEGF121, VEGF121b, VEGF145, VEGF165, VEGF165b, VEGF189, VEGF206; у грызунов ортологи этих белков содержат на одну аминокислоту меньше). Эти области имеют важные функциональные последствия для вариантов VEGF, так как сайт сплайсинга терминального участка (8-й экзон) определяет, будут ли белки проангиогенными (проксимальный сайт сплайсинга, используемый в ходе ангиогенеза) или антиангиогенными (дистальный сайт сплайсинга, используемый в нормальной ткани). Кроме того, включение или исключение 6-го и 7-го экзонов обеспечивают взаимодействия с гепарансульфатными протеогликанами и нейропилиновыми корецепторами на поверхности клетки, увеличивая их способность связывать и активировать рецепторы VEGF (VEGFR). Недавно было показано, что у мышей белок VEGF-C является важным индуктором нейрогенеза в субвентрикулярных зонах, не оказывающим ангиогенных эффектов.